Autores | Contacto
N. L. Vaquero *, C. Mussari ** y M. C. Girard Bosch ***
* Jefe Servicio Dermatoleprología. Hospital Nacional «Dr. Baldomero Sommer». General Rodríguez. Provincia de Buenos Aires.
** Bioquímica de Planta. Hospital Municipal «Bernardino Rivadavia». Laboratorio. Medicina Nuclear. Ciudad Autónoma de Buenos Aires.
*** Bioquímica Interina. Hospital Interzonal Especializado en Pediatría «Sor María Ludovica». La Plata. Provincia de Buenos Aires.
e-mail: nlvaquero@yahoo.com.ar
Dirección
Prof. Dr. Ricardo E. Achenbach
Resumen | Palabras Claves
Resumen
La enfermedad de Hansen producida por el Mycobacterium leprae, es una enfermedad infecciosa cuyo amplio espectro clínico e inmunopatológico se correlaciona con los diferentes patrones de respuesta Th1/Th2. La activación preferencial de esas subpoblaciones de linfocitos T CD4 juega un rol importante en su patogenia y constituye un modelo natural de esa dicotomía de la respuesta inmune.
Ambas formas polares de la lepra presentan un perfil definido de secreción de citoquinas: Th1 (IL2 e IFNγ) en el polo tuberculoide y Th2 (IL4, IL5, IL10) en el polo lepromatoso. En el primer caso, la respuesta celular adecuada estimula la activación macrofágica y lleva a la destrucción del bacilo. Las lesiones son escasas y limitadas a la piel y nervios periféricos. En el segundo en cambio, la respuesta celular es casi nula y los bacilos se multiplican descontroladamente dentro de los macrófagos, llevando a la diseminación de las lesiones y afectación de otros órganos. La inmunidad humoral está exacerbada y hay un alto nivel de anticuerpos que no pueden eliminar el germen intracelular.
Los factores que determinan la diferenciación hacia una respuesta Th1 ó Th2 no se han esclarecido totalmente. Se han postulado varias hipótesis que hacen referencia a factores genéticos, prevalencia de citoquinas en el microambiente celular, disfunción macrofágica; alteración en los receptores Toll de la inmunidad innata, en la expresión de moléculas coestimulatorias, etc En los últimos años se han descubierto nuevas subpoblaciones de linfocitos, (CD4+ CD25+, Tr1, Th3 y Th17) que estarían implicadas en la desregulación de estas respuestas inmunes.
Palabras clave: Lepra; Enfermedad de Hansen; Inmunopatología; Subpoblaciones linfocitarias T helper 1-T helper 2 (Th1/Th2)
Summary
Hansen’ disease, caused by Mycobacterium leprae, is an infectious illness whose wide clinical and immunopathologic spectrum correl with different Th1/Th2 responses patterns. The prefferencial activation of the CD4 T cells subset play an important rol in it’s pathogenia and provides a natural model of that balance.
Either polars forms present a defwed citokynes secretion profile: Th1 cells (IL-2 and IFN-g) dominate in tuberculoid form, whereas cytokines typically produced by Th2 cells (IL-4, IL-5 and IL-10) dominate in lepromatous form. In the first case, the macrophagic activation kills M leprae. It’s lesions are located in nerves and skin only. In the second case, cell-mediated immunity is absent. The bacilli multiply uncontrolably in macrophages and infection is widely disseminated affecting other organs. Humoral immunity is exacerbated and have high levels of antibodies that cannot reach intracellular germ.
The factors that determine whether the proliferation CD 4 T cells differentiate into Th1 or Th2 cell are not fully understood. Several hypothesis include genetics factors, prevail of cytokinesin the microenviroment, macrophagic disfunction; alterations in the coestimulatory molecules, on toll receptors of the innate immunity, etc. In recent years times new limphocytes subsets have been discovery (CD4+CD 25+, Tr1, Th3, Th17) that could be implicated in this desregulated immune reponses.
Key words: Leprosy; Hansen’disease; Immunopathology; T helper 1-T helper 2 limphocytes subsets (Th1/Th2).
Artículo | Referencias
Descargar archivo PDF aquí
Introducción
El paradigma Th1/Th2 provee un modelo útil para entender la patogenia de ciertas enfermedades, como así también el desarrollo de estrategias terapéuticas. Una de las características más llamativas de la lepra o enfermedad de Hansen, es su amplio espectro clínico e inmunopatológico, el que se correlaciona ampliamente con esos diferentes patrones de respuesta inmunológica. Si bien en los últimos años se han descubierto otras subpoblaciones linfocitarias T (Th 17, Th3 y Tr1, etc.), aquel es el modelo mejor estudiado hasta el momento en lepra y otras enfermedades con características similares.
Discusión
La lepra o enfermedad de Hansen, constituye un modelo natural que ejemplifica la dicotomía de la respuesta inmune Th1/Th2 y se traduce en manifestaciones clínicas e inmunológicas opuestas: el polo tuberculoide (T) y el polo lepromatoso (L). En medio de ambos existen formas intermediarias, llamadas borderline o dimorfas (D o B), que por su inestabilidad inmunológica tienen características no bien definidas y pueden variar dinámicamente hacia un extremo u otro del espectro (Cuadro I). Su agente etiológico, el Mycobacterium leprae, es un bacilo ácido alcohol resistente (BAAR) que se comporta como un parásito intracelular y se ubica preferentemente en los histiocitos de la piel y las células de Schwann de los nervios periféricos. En las formas más graves compromete además hígado, bazo, ojos, testículos, huesos, etc.
Cuadro I: Espectro inmunológico de la lepra
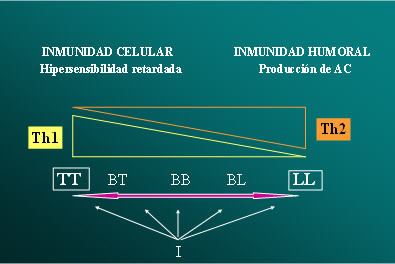
Por un lado, los pacientes con lepra tuberculoide pueden montar una respuesta celular capaz de eliminar al microorganismo y restringir el número de sus lesiones en la piel. Estas son escasas, de bordes bien delimitados, sin bacilos detectables, anestésicas y con compromiso neural de rápida instalación cuando se afecta un nervio periférico.
Muestran reacciones fuertemente positivas a la lepromina e histológicamente presentan granulomas con abundantes linfocitos, células epitelioides y ausencia de bacilos (Figs 1 y 2).
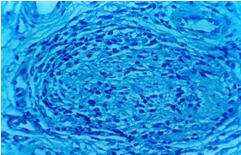
Fig 1: granuloma tuberculoide.
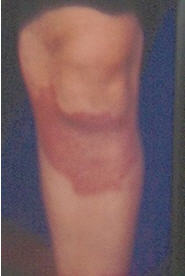
Fig 2: lesión única de LT en miembro inferior.
En el otro extremo del espectro se encuentran los pacientes con lepra lepromatosa, cuya evolución crónica y sus lesiones diseminadas a otros órganos y sistemas, son el resultado de una escasa o nula respuesta celular, responsable de la anergia que le impide controlar la enfermedad. Estos pacientes tienen una exacerbada respuesta humoral, con un alto nivel de anticuerpos circulantes. Sus lesiones son generalizadas, el compromiso neural más lento, simétrico y presentan un infiltrado predominantemente mononuclear, con abundantes macrófagos repletos de bacilos (células de Virchow) y escasos linfocitos. La reacción a la lepromina es negativa (Figs 3 y 4).
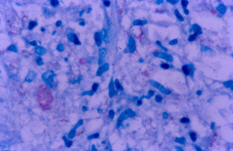
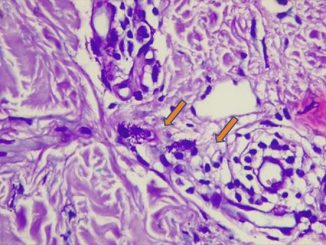
Fig 3: abundantes BAAR en LL
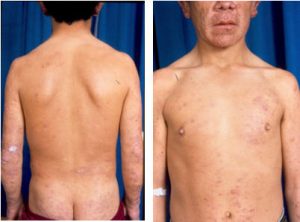
Fig 4: lesiones generalizadas en tronco, miembros y cara.
Estas formas polares de la lepra se han correlacionado con perfiles definidos de secreción de citocinas. Un perfil Th1 con la forma tuberculoide: IL-2 e INF-γ, y un perfil predominantemente Th2 con la lepromatosa: IL-4, IL-5, IL-10 1, 2. Estas manifestaciones tan disímiles de la lepra parecen depender más de las características del huésped que del microorganismo. A pesar de la dificultad que significa para su estudio, el hecho que el bacilo de Hansen no se haya podido cultivar in vitro hasta la actualidad, no existe evidencia que esas diferencias se deban a la patogenicidad o virulencia de distintas cepas. Se ha demostrado mediante estudios del patrón de fragmentos de ADN, digeridos con enzimas de restricción (RFLP) de cepas de M leprae de origen animal y humano, una extraordinaria similitud entre ellas 3. Los diferentes patrones de respuesta inmune dependen de múltiples factores que incluyen no sólo la naturaleza y concentración del antígeno, sino también de las condiciones que predominan en el microambiente celular inmediato y de la capacidad funcional del huésped para responder.
El bacilo de la lepra es de baja patogenicidad. Puede haber en las lesiones de la forma lepromatosa, una alta carga bacilar sin evidencia de daño tóxico. La patología de esta enfermedad refleja en gran parte, la consecuencia de la respuesta inmunológica del huésped que ocasiona el daño tisular, por mecanismos de hipersensibilidad, puestos de manifiesto especialmente durante el transcurso de los episodios agudos reaccionales: reacciones de hipersensibilidad retardada en las formas borderline del espectro (reacciones Tipo 1) y por inmunocomplejos en el caso de los lepromatosos o cercanos a ese polo (reacciones Tipo 2). En las primeras, llamadas reacciones reversales (RR) existe un aumento de la actividad bactericida y reducción de la carga bacteriana a partir del incremento en la producción de citocinas proinflamatorias con el consiguiente daño, sobre todo a nivel neural, al que también contribuiría un proceso de autoinmunidad, debido a la formación de neoantígenos en el sitio de inflamación 4. Las reacciones tipo 2 en cambio (eritema nudoso leproso o ENL, eritema polimorfo, vasculitis necrotizante) son el resultado de una inadecuada respuesta humoral con la presencia de inmunocomplejos, complemento y polinmorfonucleares que frecuentemente producen vasculitis de diferente magnitud en individuos bacilíferos. De todas maneras, varios trabajos han implicado un aumento de la IMC específica o no específica como factor desencadenante en el ENL 5. El TNF liberado por los macrófagos intervendría en la patogénesis de las lesiones, lo que se vería reflejado en la eficacia de la talidomida (medicamento que bloquea la liberación de esta citocina) en estos casos 6,7.
Los factores que confieren resistencia o susceptibilidad al huésped no son bien conocidos. Dentro de ellos se han considerado los relacionados a antígenos de histocompatibilidad, asociándose ciertos genes y el tipo de lepra desarrollado (HLA-DR en T y HLA-DQ1 en L). Investigaciones más recientes observaron que el tipo de lepra resultante puede estar asociado a otros genes como el Nramp-1 (natural resistance associated macrophage protein 1) cuyos niveles estarían disminuidos en pacientes lepromatosos debido a la baja expresión de IRF-8, un factor de transcripción específico del macrófago que participa en la expresión regulada de las citocinas proinflamatorias IL12, IL18 e IL1β 8.
Se han postulado varias hipótesis para explicar la incapacidad de un individuo con lepra lepromatosa, para responder contra los antígenos del M leprae (anergia celular): carencia de linfocitos reactivos, sobreactivación de células supresoras, presentación defectuosa del antígeno por las APCs, deficiente expresión de las moléculas coestimulatorias, falla en la producción de citoquinas pro inflamatorias o sus receptores, actividad excesiva de células productoras de citoquinas antiinflamatorias, etc. 9.
Los primeros estudios sistemáticos sobre la inmunología de la lepra han encontrado un número disminuido de LT y respuestas linfoproliferativas ante el estímulo con lepromina, concavalina-A (Con-A) y fitohamaglutinina (PHA) en los pacientes lepromatosos respecto de los tuberculoides y la población sana, sugiriendo que esto se debía a una actividad supresora. Posteriormente, mediante anticuerpos monoclonales contra células supresoras (OKT8+/Leu2a+) y contra células cooperadoras (OKT4+/Leu3a+), se estableció que en los granulomas de lepra tuberculoide predominan células OKT4+ entre las células epiteliodes y las OKT8+ forman un manto periférico. En los lepromatosos predominan las OKT8+ que se entremezclan con los macrófagos de toda la lesión 10,11. En esa época se lograron aislar y clonar células T cooperadoras (Th) y supresoras (Ts), de un paciente borderline lepromatoso (BL) en los cuales las Ts suprimían la respuesta proliferativa de las Th, inducida por una proteína de 36 KD del M leprae, a la que se le adjudicó la responsabilidad de la supresión 12.
También se realizaron estudios sobre la función macrofágica en los pacientes hansenianos y se encontraron factores solubles derivados de los monocitos de pacientes lepromatosos, pero no de tuberculoides, con actividad supresora (MoFs). Algunos autores sostienen que contienen IL10 y PGE, reconocidos inhibidores de la síntesis de citoquinas pro inflamatorias 13, contrariamente a lo afirmado por otras comunicaciones previas 14. Se ha sugerido que la PGE favorece el desarrollo de citoquinas Th2, tanto por la inhibición de la producción de la IL12 por las APCs, como por la producción de IFNγ por las células T. Respecto de la producción de IL1, varios estudios llegaron a la conclusión que la incapacidad de los leucocitos de los pacientes lepromatosos de proliferar en respuesta al M leprae, no se debe a un defecto en su producción por los monocitos de los pacientes, sino a algún defecto u otro nivel 15. El posterior hallazgo en suero de altos títulos del receptor de IL1 en estos pacientes (sIL1R) podría ser la causa, ya que neutralizarían a la IL1 impidiendo su estimulación sobre las células T 16.
Investigaciones recientes sostienen que las citoquinas Th1 incrementan la expresión de los receptores Toll 1 (TLR1), mientras que las Th2 deprimen la expresión de los de tipo 2 (TLR 2) y que la expresión de ambos es más marcada en las lesiones de lepra tuberculoide que en las de la lepromatosa 17. Bochud y col 18 encontraron que los pacientes con lepra lepromatosa muestran una alta frecuencia de expresión de la variante TLR 2Arg (677)Trp y que la presencia de este polimorfismo en los TLR 2 suprime en los macrófagos, la activación de NFκB y la síntesis de TNFα en presencia de M leprae , lo que también podría explicar la pobre respuesta celular de la lepra lepromatosa.
Sobre la base que la lepra tuberculoide tiene un patrón de respuesta Th1 (IL2, IFNγ) mientras que la lepromatosa, Th2 (IL4, IL6, IL10, TGFβ) algunos autores propusieron que la anergia en las formas lepromatosas, se debería a un defecto en la expresión de IL12, ya que esta es fundamental para la expresión de citocinas Th1 2,19. Observaron que los pacientes con lepra tuberculoide expresan una cantidad diez veces mayor de IL12 que los lepromatosos y que in vitro; la IL12 recombinante favorece la proliferación las células T en estos últimos, inducida por M leprae, así como la liberación de IFNγ por estas células. Sin embargo, otros autores contradicen esto último y a través de estudios inmunohistoquímicos adjudican la falta de respuesta a la IL12 exógena, a una falla en la señal de transducción originada en una expresión defectuosa de la cadena beta-2 del receptor para IL12 (IL-12Rβ2) 20.
También son contradictorios los resultados respecto de la falta de producción IL2 en la forma lepromatosa y los resultados del su agregado en forma exógena. Nuevamente el defecto se explicaría por una alteración en la expresión de su receptor (IL2R), que no permitiría reconstituir la respuesta in vivo 21. En forma similar, estos autores encontraron que los leucocitos de los pacientes lepromatosos no secretan IFNγ cuando se estimulan con M leprae, en contraposición con los pacientes tuberculoides y propusieron que la anergia se debería a la falta de IL2, como ya se mencionó.
Estableciendo líneas celulares T a partir de células mononucleares de sangre periférica (CMP), para estudiar el perfil de citocinas de leucocitos T reactivos para M leprae, se encontró que las micobacterias inducen altos títulos de IFNγ y TNFα en todo el espectro de la lepra, aunque algunos de los clones T podían producir al mismo tiempo IL4 e IFNγ (Th0) 22. Otros investigadores 23 publicaron el perfil de secreción de citocinas de CMP obtenidas de pacientes con lepra, determinado por RT-PCR y confirmado por ELISA. En este estudio el 40 a 50 % de todos los individuos presentaron un perfil mixto tipo Th0, independientemente de la clasificación clínica de los pacientes. Otros autores 24 evaluando la producción de citocinas por CMP, estimuladas con Con-A, M leprae y PPD tampoco encontraron una clara asociación entre el perfil de citocinas evaluadas y la forma clínica. Esto difiere de los resultados obtenidos con linfocitos recuperados de las lesiones, diferencia que los autores atribuyen a la presencia de otras células en estas últimas, respecto de la población circulante. Estas (macrófagos, células dendríticas) podrían alterar el perfil de citocinas en cultivos reconstituidos, lo que sugiere su importancia en la diferenciación de subpoblaciones de linfocitos T cooperadores.
Respecto de la citoquina TGFβ también existen controversias. Algunos investigadores refieren su presencia en la forma lepromatosa, 25 mientras que otros lo niegan 1. Aparentemente, gran cantidad de antígeno bacteriano estimularía la expresión de los niveles de TGFβ y como consecuencia, habría una supresión de la actividad de los macrófagos. El balance entre TGFβ y citoquinas pro inflamatorias como el TNFα, podría orientar sobre el estado clínico del paciente. Altos niveles de TNFα en asociación con niveles bajos de TGFβ, indicarían riesgo de presentar un episodio reaccional. Además, el TGFβ regula la producción de IL1, IL6 y TNFα que se encuentran en mayor proporción en los pacientes con estado reaccional tipo 2 (ENL) 26,27.
Otras hipótesis para dilucidar las diferencias en los patrones de citoquinas en las formas polares de la lepra, es el de una defectuosa presentación antigénica por los macrófagos, originada en una falla en la expresión de las moléculas coestimulatorias CD40-CD40 L 28 , en la interacción B7-CD28 29 y más recientemente, en la molécula SLAM (molécula linfocitaria activadora de señales), receptor glicoproteico de superficie que participa en la estimulación T, aumenta la producción de IFN.γ y la proliferación celular 30 . Otro factor que modula el patrón de citoquinas producidas por las células T estudiado por el mismo grupo de investigadores, es la proteína asociada a SLAM (SAP) que actúa como un inhibidor natural de las vías de transducción de señales, desde SLAM hacia el interior de la célula. Estudios recientes sugieren que los pacientes con lepra lepromatosa presentan un incremento en la expresión de ARNm de SAP, lo que impide la producción de IFNγ, contrariamente a lo que ocurre en las formas tuberculoides 30. No obstante todo lo expuesto anteriormente, también es probable que la diferencia en el patrón de citoquinas en la lepra, puede deberse a la actividad de otras células con función reguladora mencionadas anteriormente (T CD4+CD25+, Tr1, Th3), que ejercen su acción moduladora a través de la secreción de citoquinas antiinflamatorias IL4, IL10, TGFβ. Su participación en la patología de la lepra todavía no se ha explorado en profundidad.
Concluyendo, la diferente respuesta inmunológica en los pacientes con enfermedad de Hansen es un fenómeno complejo y multifactorial, que depende de alteraciones de la red de interacciones celulares y moleculares que componen la respuesta inmunitaria. El descubrimiento de los mecanismos intrínsecos de la misma permitiría una mejor comprensión de su patogenia y el desarrollo de nuevas estrategias terapéuticas.
1. Yamamura, M., Uymemura, K., Deans, R. J. y col. Defining protective response to infectious pathogens: cytokine profiles in leprosy lesions. Sciencie 1991; 254: 277-279.
2. Modlin, R. Th1-Th2: Insights from leprosy. J Invest Dermatol 1994; 102 (6): 828-832.
3. Clark Curtis, J. E. y Wash, J. P. Conservations of genomic sequences among isolates of Mycobacterium leprae. J Bacteriol 1989; 171: 484-485.
4. Spierings, E., Boer, T., Zulianello, L. y Ottenhoff, T. Novel mechanisms in the immunopathogenesis of leprosy nerve damage: The rol of Schwann cells, T cells and Mycobacterium leprae. Immunol Cell Biol 2000; 78: 349-355.
5. Rea,T. H. y Sieling, P. A. Delayed-type hypersensitivity reactions followed by erithema nodosum leprosum. Int J Lepr 1998; 66: 316-327.
6. Ulrich, M. Inmunología de la lepra. Dermatol Venezol 1994; 32: 167-170.
7. Sampaio, E. P., Sarno, E. N., Galilly, R. y col. Thalidomide selectively inhibits tumour-necrosis factor production by stimulated human monocytes. J Exp Med 1991; 173: 699-703.
8. Alter Koltunof, M., Ehric, S., Dror, N. y col. N-ramp-1 mediated innata resistance to intraphagosomal pathogens is regulated by IRF8, PU 1 and Miz-1. J Biol Chem 2003; 278: 44025-44032.
9. Rojas Espinosa, O. Anergia en lepra. ¿Dónde está el defecto? Fontilles Rev Leprol 2007; 26 (2): 121-142.
10. Van Boris, W. C., Kaplan, G., Sarno, E. N. y col. The cutaneous infiltrates of leprosy: cellular characteristics and the predominant T-cell phenotypes. N Engl J M 1982; 307: 1593-1597.
11. Modlin, R. L., Hoffman, F. M., Taylor, C. R. y Rea, T. H. T limphocyte subsets in the skin lesions of patients with leprosy. J Am Acad Dermatol 1983; 8: 182-189.
12. Ottenhoff, T. H., Elferink, D. G., Klaster, P. R. y de Vries, R. R. Cloned supresor T cells. Nature 1986; 322: 459-461.
13. Misra, N., Selvakumar, M., Singh, S. y col. Monocyte derived IL-10 and PGE2 are associated with the absense of Th1 cells and in Vitro T cells supressión in lepromatous leprosy. Immunol Lett 1995; 48: 123-128.
14. Sathis, M., Bhutani, L. K., Sharma, A. K. y Nath, I. Monocyte derived soluble supressor factors in patients with lepromatous leprosy. Infect Immunol 1983; 42: 890-899.
15. Ridel, P. R., Famet, P., Robin, Y. y Bach, M. A. Interleukin-1 released by blood- monocyte- derived macrophages from patients with leprosy. Infect Immunol 1986; 25: 303-308.
16. Fafutis Morris, M., Guillén Vargas, C. M., Navarro Fierro, S. y col. Serum sIL-1R is elevated in lepromatous leprosy patients. Int J Lepr Other Mycobact Dis 1999; 67: 287-291.
17. Krutzik, S. R., Ochoa, M. T., Sieling, P. A. y col. Activation and regulation of Toll-like receptors 2 and 1 in human leprosy. Nat Med 2003; 9: 525-532.
18. Bochud, P. Y., Hawn, T. R. y Aderem, A. Cutting edge: A toll-like receptor 2 polymorphism that is associated with lepromatous leprosy is unable to mediate mycobacterial signalling. J Immnol 2003; 170: 3451-3454.
19. Sieling, P. A., Wang, X. H., Gately, M. K. y col. IL12 regulates T helper Type 1 cytokine responses in human infectious diseases. J Immunol 1994; 153: 3639-3647.
20. Kim, J., Uyemura, K., Van Dike, M. K. y col. A role for IL12 receptor expression and signal transdiction in host defense in leprosy. J Immunol 2001; 167: 779-786.
21. Mohaghegpour, N., Gelber, R. H., Larrick, J. W. y col. Defective cell-mediated immunity in leprosy: failure of T cells from lepromatous leprosy patients to respond to Mycobacterium leprae associated with defective expression of interleukin-2 receptors and is not reconstituted by interleukin 2. J Immunol 1985; 135: 1443-1449.
22. Mutis, T., Kraakman, E. M., Cornelisse, Y. E. y col. Analysis of citokine production by Mycobacterium –reactive T cells. J Immunol 1993; 150: 4641-4651.
23. Misra, N., Murtaza, A., Walter, B. y col. Citokine profile of circulating T cells in leprosy patients reflects both indiscriminated and polarized T-helper subsets. Immunol 1995; 86: 97-103.
24. Fink,S., Finíais, M., Valdéz, R., De la Barrera, S. y Sasiaini, M. C. Evaluación de la producción de citoquinas en enfermos de lepra. http://www.medicinabuenosaires.com/vol56 96/6producciondecitoquinas.htm.
25. Goularr, I. M. B., Figueiredo, F., Coimbra, T. y Foss, N. T. Detection of transforming growth factor-beta 1 in termal lesions of different clinical forms of leprosy. Am J Pathol 1996; 148: 911-917.
26. Rada, E., Aranzazu, N. y Convit, J. Ciertos aspectos inmunológicos en los estados reaccionales en la enfermedad de Hansen. Invest Clin 2005; 46 (4): 381-389.
27. Goulart, I. M. B., Mineo, J. R. y Foss, N. T. Production of transforming growth factor beta 1 by blood monocytes from patients with different clinical form of leprosy. Clin Exp Immunol 2000; 122: 330-334.
28. Yamauchi, P. S., Bleharsky, J. R., Uyemura, K. y col. A role of CD40 –CD40L ligands interactions in the generation of type 1 citokine response in human leprosy. J Immunol 2000; 165: 1506-1512.
29. Agrewala, J. N., Kumar, B., y Vohra, H. Potencial role of B7-1 and CD28 molecules in immunosupression in leprosy. Clin Exp Immunol 1998; 111: 56-63.
Referencias
Referencias
1. Yamamura, M., Uymemura, K., Deans, R. J. y col. Defining protective response to infectious pathogens: cytokine profiles in leprosy lesions. Sciencie 1991; 254: 277-279.
2. Modlin, R. Th1-Th2: Insights from leprosy. J Invest Dermatol 1994; 102 (6): 828-832.
3. Clark Curtis, J. E. y Wash, J. P. Conservations of genomic sequences among isolates of Mycobacterium leprae. J Bacteriol 1989; 171: 484-485.
4. Spierings, E., Boer, T., Zulianello, L. y Ottenhoff, T. Novel mechanisms in the immunopathogenesis of leprosy nerve damage: The rol of Schwann cells, T cells and Mycobacterium leprae. Immunol Cell Biol 2000; 78: 349-355.
5. Rea,T. H. y Sieling, P. A. Delayed-type hypersensitivity reactions followed by erithema nodosum leprosum. Int J Lepr 1998; 66: 316-327.
6. Ulrich, M. Inmunología de la lepra. Dermatol Venezol 1994; 32: 167-170.
7. Sampaio, E. P., Sarno, E. N., Galilly, R. y col. Thalidomide selectively inhibits tumour-necrosis factor production by stimulated human monocytes. J Exp Med 1991; 173: 699-703.
8. Alter Koltunof, M., Ehric, S., Dror, N. y col. N-ramp-1 mediated innata resistance to intraphagosomal pathogens is regulated by IRF8, PU 1 and Miz-1. J Biol Chem 2003; 278: 44025-44032.
9. Rojas Espinosa, O. Anergia en lepra. ¿Dónde está el defecto? Fontilles Rev Leprol 2007; 26 (2): 121-142.
10. Van Boris, W. C., Kaplan, G., Sarno, E. N. y col. The cutaneous infiltrates of leprosy: cellular characteristics and the predominant T-cell phenotypes. N Engl J M 1982; 307: 1593-1597.
11. Modlin, R. L., Hoffman, F. M., Taylor, C. R. y Rea, T. H. T limphocyte subsets in the skin lesions of patients with leprosy. J Am Acad Dermatol 1983; 8: 182-189.
12. Ottenhoff, T. H., Elferink, D. G., Klaster, P. R. y de Vries, R. R. Cloned supresor T cells. Nature 1986; 322: 459-461.
13. Misra, N., Selvakumar, M., Singh, S. y col. Monocyte derived IL-10 and PGE2 are associated with the absense of Th1 cells and in Vitro T cells supressión in lepromatous leprosy. Immunol Lett 1995; 48: 123-128.
14. Sathis, M., Bhutani, L. K., Sharma, A. K. y Nath, I. Monocyte derived soluble supressor factors in patients with lepromatous leprosy. Infect Immunol 1983; 42: 890-899.
15. Ridel, P. R., Famet, P., Robin, Y. y Bach, M. A. Interleukin-1 released by blood- monocyte- derived macrophages from patients with leprosy. Infect Immunol 1986; 25: 303-308.
16. Fafutis Morris, M., Guillén Vargas, C. M., Navarro Fierro, S. y col. Serum sIL-1R is elevated in lepromatous leprosy patients. Int J Lepr Other Mycobact Dis 1999; 67: 287-291.
17. Krutzik, S. R., Ochoa, M. T., Sieling, P. A. y col. Activation and regulation of Toll-like receptors 2 and 1 in human leprosy. Nat Med 2003; 9: 525-532.
18. Bochud, P. Y., Hawn, T. R. y Aderem, A. Cutting edge: A toll-like receptor 2 polymorphism that is associated with lepromatous leprosy is unable to mediate mycobacterial signalling. J Immnol 2003; 170: 3451-3454.
19. Sieling, P. A., Wang, X. H., Gately, M. K. y col. IL12 regulates T helper Type 1 cytokine responses in human infectious diseases. J Immunol 1994; 153: 3639-3647.
20. Kim, J., Uyemura, K., Van Dike, M. K. y col. A role for IL12 receptor expression and signal transdiction in host defense in leprosy. J Immunol 2001; 167: 779-786.
21. Mohaghegpour, N., Gelber, R. H., Larrick, J. W. y col. Defective cell-mediated immunity in leprosy: failure of T cells from lepromatous leprosy patients to respond to Mycobacterium leprae associated with defective expression of interleukin-2 receptors and is not reconstituted by interleukin 2. J Immunol 1985; 135: 1443-1449.
22. Mutis, T., Kraakman, E. M., Cornelisse, Y. E. y col. Analysis of citokine production by Mycobacterium –reactive T cells. J Immunol 1993; 150: 4641-4651.
23. Misra, N., Murtaza, A., Walter, B. y col. Citokine profile of circulating T cells in leprosy patients reflects both indiscriminated and polarized T-helper subsets. Immunol 1995; 86: 97-103.
24. Fink,S., Finíais, M., Valdéz, R., De la Barrera, S. y Sasiaini, M. C. Evaluación de la producción de citoquinas en enfermos de lepra. http://www.medicinabuenosaires.com/vol56 96/6producciondecitoquinas.htm.
25. Goularr, I. M. B., Figueiredo, F., Coimbra, T. y Foss, N. T. Detection of transforming growth factor-beta 1 in termal lesions of different clinical forms of leprosy. Am J Pathol 1996; 148: 911-917.
26. Rada, E., Aranzazu, N. y Convit, J. Ciertos aspectos inmunológicos en los estados reaccionales en la enfermedad de Hansen. Invest Clin 2005; 46 (4): 381-389.
27. Goulart, I. M. B., Mineo, J. R. y Foss, N. T. Production of transforming growth factor beta 1 by blood monocytes from patients with different clinical form of leprosy. Clin Exp Immunol 2000; 122: 330-334.
28. Yamauchi, P. S., Bleharsky, J. R., Uyemura, K. y col. A role of CD40 –CD40L ligands interactions in the generation of type 1 citokine response in human leprosy. J Immunol 2000; 165: 1506-1512.
29. Agrewala, J. N., Kumar, B., y Vohra, H. Potencial role of B7-1 and CD28 molecules in immunosupression in leprosy. Clin Exp Immunol 1998; 111: 56-63.