Autores | Contacto
CI Rico *, J Rodríguez **, CA Conde ***, JC Mantilla **** y P Escobar *****
* Bióloga. Candidata a Título de Maestría en Ciencias Básicas Biomédicas. Universidad Industrial de Santander.
** Ingeniero Agrónomo. Técnico Bioterio Central. Universidad Industrial de Santander.
*** Médico Neurofisiólogo M.Sc.PhD. Docente. Universidad Industrial de Santander.
**** Médico Patólogo. Docente. Universidad Industrial de Santander.
***** Bacterióloga. M.Sc.PhD. Docente. Universidad Industrial de Santander.
Centro de Investigación en Enfermedades Tropicales (CINTROP). Departamento de Ciencias Básicas. Escuela de Medicina. Universidad Industrial de Santander. Piedecuesta. Santander. Colombia. Km 2 vía al Refugio, Sede UIS Guatiguará. Tel/Fax: +57-7 6344000 Ext 3550.
E-mail: pescobarwww@yahoo.co.uk
Dirección
Prof. Dr. Ricardo E. Achenbach
Resumen | Palabras Claves
RESUMEN
Una formulación tópica en leishmaniasis cutánea debe garantizar la permeación y acumulación del compuesto en la dermis, sitio donde se encuentran los macrófagos infectados con Leishmania. Se determinó la difusión y retención de PcAlCl contenida en una nanoemulsión (nano-PcAlCl) y en solución-PcAlCl y su distribución en ratas Wistar, con piel sana o lesionada quirúrgicamente. La nano-PcAlCl se preparó por el método de emulsificación espontánea y la solución-PcAlCl en mezcla DMSO: Tween 80: agua tipoI; la estabilidad se determinó espectrofotométricamente. La difusión se determinó utilizando celdas de Franz y la retención en el estrato córneo (EC) y la epidermis-dermis (E+D) por «tape stripping». Las formulaciones mantuvieron las características espectroscópicas del compuesto. La PcAlCl no difundió al medio receptor. Después de 12 y 24 horas la retención del compuesto en EC con nano-PcAlCl fue 99,73 y 79,40nM y con solución-PcAlCl 66,73 y 57,01nM; en E+D la retención con nano-PcAlCl fue 40,94 y 62,49nM y con solución-PcAlCl 81,92 y 50,28nM. En EC la nano-PcAlCl registró mayor retención y en E+D la solución-PcAlCl, registró mayor retención a las 12 horas y la nano-PcAlCl a las 24 horas. Se observó desprendimiento y disminución en las capas del epitelio.
El tratamiento con nano-PcAlCl retuvo el compuesto en EC y E+D de los animales con valores de 6,43nM y 33,18nM con piel sana y 0,99nM y 17,08 con piel lesionada; valores menores de 1,92nM fueron detectados sólo en pulmón. El tratamiento con solución-PcAlCl retuvo el compuesto en EC y E+D de los animales con valores de 31,86 y 202,40nM con piel sana y 5,93 y 63,83nM con piel lesionada; se encontraron valores de 2,36nM y 20,33nM en los pulmones y valores entre 1,58 y 5,80nM en otros órganos. La piel lesionada presentó regeneración del epitelio, desprendimiento de queratina, infiltrado celular y neovascularización. La PcAlCl retenida en EC y E+D indicó la eficacia de las formulaciones para penetrar el EC y retener el compuesto en las capas viables de la piel. El tratamiento con nano-PcAlCl permeó el EC, se retuvo en E+D y no presentó distribución hacia órganos.
PALABRAS CLAVE: Nanoemulsión; Ftalocianina de aluminio clorada; Celdas de difusión de Franz; Permeación en piel; Biodistribución; Leishmaniasis cutánea.
SUMMARY
A successful formulation contained aluminum phthalocyanine chloride (ClAlPc) able for cutaneous leishmaniasis (CL) ensures the skin permeation and retention of the compound in dermis, a place where macrophages infected with Leishmania are located. The aim of this study was to determine the ClAlPcex vivo permeation and retention in Wistar rat skin and its distribution in animals with healthy skin and surgically damaged skin. Two formulations were prepared: nanoemulsion (ClAlPc-nano) and solution (ClAlPc-solution). The diffusion was determined using Franz diffusion cells with Wistar rat skin as membrane after 12 and 24 hours of testing. Retention in stratum corneum (SC) and epidermis plus dermis (E+D) was determined by the tape stripping method and organic solvent extraction. The distribution was performed after the topical application of formulations analyzing the CLAlPc concentration in the skin layers and organs by fluorometry. The results were expressed as nM/mg of tissue of ClAlPc. Simultaneously, skin biopsies were taken in order to determine their histological characteristics. ClAlPc formulations were effective in maintaining compound solubility and spectroscopic characteristics. ClAlPc was unable to pass completely through the skin; its skin retention was related with the used formulation, time of assays and type of skin layer. After 12 and 24 hours, the SC retention induced by ClAlPc-nano treatment was 99.73 and 79.40nM and by ClAlPc-solution was 66.73 and 57.01nM. In E+D the retention induced by ClAlPc-nano was 40.94 and 62.49nM and by ClAlPc-solution was 81.92 and 50.28nM. In SC, ClAlPc-nano showed greater retention after 12 and 24 hours, while in E+D, ClAlPc-solution was greater retained at 12 hours and ClAlPc-nano at 24 hours. After the permeation assays, detachment and reduction in epithelial layers were observed in skin membranes. In Wistar rats, ClAlPc-nano placed on healthy skin retained the compound in E+D and SC with values of 33.18nM and 6.43nM and placed on damaged skin retained in E+D in SC with values of 17.08nM and 0.99nM respectively; no organs distribution occur, except in lung where values of 0.82nM in animals with healthy skin and 1.92nM in animals with damaged skin were observed. ClAlPc-solution induced retention of 31.86 in SC and 202,40nM in E+D placed on healthy skin and 5.93 in SC and 63.83nM E+D placed on damaged skin; concentrations in lung with values of 2,36nM after application in animals with healthy skin and 20,33nM in animals with damaged skin were observed. In addition, ClAlPc-solution promoted, after application on damaged skin, distribution of ClAlPc to other organs with values between 1.58 and 5.80nM. In animals without skin injury, normal histologic skin anatomy were observed after treatment. In contrast, epithelial regeneration, detachment of keratin, loss of cellular differentiation, cellular infiltration and neovascularization were observed in animals with skin injury. The efficacy of the formulation to penetrate the SC and be retained in the viable skin layers was demonstrated. The in vivo ClAlPc-biodistribution was related on its concentration and skin state. A nanoemulsion contained ClAlPc, represents a good system of drug delivery because induce both the SC penetration and E+D retention, without systemic organ distribution even when presented tissue repair and regeneration. A ClAlPc-nano prepared in this work constitutes a good formulation for the topical application of ClAlPc in LC treatment.
KEY WORDS: Nanoemulsion; Choroaluminum phthalocyanine; Franz diffusion cells; Skin permeation; Biodistribution; Cutaneous leishmaniasis.
Artículo | Referencias
Descargar archivo PDF aquí
INTRODUCCIÓN
La farmacología dermatológica consiste en la aplicación de fármacos sobre la piel, para el tratamiento de enfermedades que la afectan; estos preparados terapéuticos son utilizados con el fin de restaurar la apariencia y la fisiología normal de este tejido 1,2. La evaluación de la absorción percutánea de moléculas, es un importante paso en el desarrollo y optimización de formulaciones tópicas 3. La permeación de la piel está asociada con la integración directa entre el compuesto y el estrato córneo (EC) 4; esta capa de la piel es una barrera eficaz contra el ambiente externo, controla el flujo de componentes y actúa como la primera capa de la piel con un alto potencial lipofílico 5. El EC se representa como una red en donde los corneocitos, ricos en queratina están dentro de la matriz intercelular provista de lípidos. A partir de esta organización se da la permeación dérmica de compuestos a través de las vías transcelular, intercelular y mediante anexos cutáneos 6,7. Para muchos compuestos el EC es la principal barrera de permeación, sin embargo, la difusión a través de la epidermis viable y la dermis, capas hidrofílicas, también puede ser limitante, especialmente para compuestos lipofílicos cuando el EC está dañado o afectado 6. En enfermedades cutáneas es indispensable una mayor penetración del EC y una adecuada bioacumulación en las capas de la piel, para terapias más eficientes 4. Los tratamientos dérmicos y transdérmicos constituyen una alternativa en leishmaniasis cutánea (LC). Las leishmaniasis son un conjunto de enfermedades producidas por diferentes especies de Leishmania 8. La OMS indica que 350 millones de personas están en riesgo de leishmaniasis. La LC es la forma clínica más frecuente con una incidencia anual entre 1 y 1,5 millones de casos 9. Las manifestaciones clínicas de LC incluyen aparición de úlceras redondeadas, de bordes elevados, eritematosos, únicas o múltiples, con compromiso linfático y adenopatía 10. La respuesta inmune está mediada por células; se observa inicialmente un infiltrado dérmico denso y difuso, compuesto por histiocitos, linfocitos y células plasmáticas y en menor cantidad neutrófilos y eosinófilos 8,11; pueden observarse amastigotes dentro de los macrófagos y en el espacio extracelular. Se forman granulomas epitelioides en la dermis; la epidermis muestra hiperqueratosis y acantosis y ocasionalmente paraqueratosis y atrofia 11. Los fármacos de primera opción para el tratamiento de leishmaniasis son los antimoniales pentavalentes de aplicación sistémica (Pentostám® y Glucantime®) 12. El tratamiento de segunda elección incluye el Isotianato de Pentamidina (Pentacarinat®). Otros fármacos utilizados son la Anfotericina B (Fungizone®), la miltefosina (Impavido®) y formulaciones lipídicas de Anfotericina B 13. Debido a los efectos colaterales que presentan los tratamientos actuales para la LC como baja eficacia, toxicidad, resistencia, dificultades en la administración y alto costo, el desarrollo de un tratamiento tópico, efectivo y seguro es prioritario. Los tratamientos tópicos para la LC son una importante alternativa dado que se facilita su administración, se trata la lesión de forma localizada y se evitan efectos tóxicos 12,14; estos tratamientos pueden ser fármacos, tratamientos físicos o la combinación de ambos. Los tratamientos con fármacos incluyen la paromomicina en cremas y ungüentos 15,16 e inyecciones intralesionales de antimoniales pentavalentes 17. La terapia física incluye cauterización, escisión quirúrgica, crioterapia, termoterapia y terapia fotodinámica (TFD) 14,18,19. La TFD consiste en la administración de un fotosensibilizador (FS), seguida de la iluminación con luz visible en el sitio de la lesión, que en presencia de oxígeno molecular conduce a la liberación de especies reactivas de oxígeno (ERO), desencadenan muerte celular y destrucción de tejidos 20. La TFD ha sido aplicada con éxito en el tratamiento de enfermedades locales y tópicas como degeneración macular, lesiones de la piel, cáncer 14, 21, 22 y en la erradicación de parásitos Leishmania utilizando FS como porfirinas, ácido aminolevulínico (ALA) y protoporfirina IX 23. Se han investigado otros FS en TFD como las ftalocianinas, cuya estructura está basada en las porfirinas y generalmente incluyen un átomo central metálico como el zinc, silicio o aluminio para aumentar la producción de ERO, presentan altos niveles de absorción en el rango de 670 nm y tienen capacidades fluorescentes 24. La ftalocianina de aluminio clorada (PcAlCl) es un eficiente FS en TFD, es parcialmente soluble en agua y altamente citotóxica contra el tejido blanco después de la TFD 25. Se ha determinado que promastigotes de L (V) panamensis, L. chagasi (syn L infantum) y L (Leishmania) amazonensis son fotosensibles a la TFD utilizando PcAlCl 19,26. Este FS también ha sido utilizado tópicamente y ha mostrado ser activo en hámsters con LC 27. A pesar del conocimiento de aspectos fotofísicos y fotoquímicos de la PcAlCl, hay una lenta evolución en el estudio de su comportamiento y distribución en membranas y sistemas biológicos a partir de formulaciones tópicas. En este contexto, se reporta el estudio de Kyriazi y col 28, en el que se examinó la farmacocinética de PcAlCl en un modelo murino de piel normal y carcinoma de piel no melanoma, obteniendo resultados positivos de absorción y penetración de PcAlCl en el tejido tumoral. El diseño de formulaciones tópicas teniendo en cuenta las propiedades de barrera de la piel, requiere el uso de sistemas adecuados para que el compuesto penetre el EC y sea retenido en el sitio terapéutico. La nanotecnología brinda la posibilidad de obtener sistemas biocompatibles a escala nanométrica, con capacidad de transportar y entregar un principio activo al sitio blanco. Varios sistemas de liberación de drogas como liposomas 29, nanopartículas 30 y nanoemulsiones (NE) 31 han sido utilizados en formulaciones tópicas. Las NE son dispersiones de aceite y agua, termodinámicamente estables, presentan tamaños de gota entre 10 y 100 Nm, son generados espontáneamente, pueden ser producidos a gran escala sin necesidad de alta energía de homogeneización, solubilizan compuestos lipofílicos y son altamente biocompatibles 32. Se han llevado a cabo diversos estudios de incorporación de fármacos tópicos en NE y se ha observado incremento en la tasa de permeación y mejores efectos tópicos 33.
OBJETIVO
En este trabajo se determinó la difusión, retención y biodistribución de PcAlCl en piel de ratas Wistar, a partir de la aplicación tópica de una NE y una solución, con el fin de evaluar la capacidad de estos sistemas para permitir la penetración del EC y la acumulación del compuesto en la dermis, donde se encuentran los macrófagos parasitados 34. Este estudio es la base para la aplicación de TFD con nano-PcAlCl en el tratamiento de LC, por lo que se aportó el conocimiento respecto de la capacidad del nanosistema utilizado, la localización del compuesto en las capas de la piel y su posible biodistribución, ya que, estos son principios fundamentales de la TFD tópica.
MATERIALES Y MÉTODOS
Reactivos:
Para la preparación de las formulaciones se utilizaron los siguientes reactivos: PcAlCl, Tween 20 y Tween 80 (Sigma-Aldrich®, St. Louis, MO, USA), glicerol (Mallinckrodt, México), fosfatidilcolina (Phospholipon, PL90, Phospholipid, Alemania), cloroformo (Merck, Darmstadt, Alemania) ácido oleico (Panreac, Barcelona) y dimetilsulfóxido (DMSO, Carlo Erba Reagenti, Rodano, Italia). Otros reactivos utilizados fueron: dodecilsulfato sódico (SDS, de J. T. Baker®, USA) y etanol (Laboratorios Productos OSA, USA). El anestésico Xilacina fue adquirido de Rompun® MR,Bayer, Kiel, Alemania, laketamina® 50 de Holliday-Scott S.A. y la Vetalgina® (Dipirona) de Intervet International, Munchen, Alemania.
Formulaciones:
La NE (nano-PcAlCl) se preparó mediante técnicas de ultrasonicación mezclando una fase acuosa y una oleosa. Para la fase acuosa se utilizó agua tipo I, glicerol y Tween 20. Para la fase oleosa se utilizó fosfatidilcolina, PcAlCl diluida en cloroformo y ácido oleico. La solución de PcAlCl (solución-PcAlCl) se preparó disolviendo la PcAlCl en DMSO, Tween 80 y agua tipo I (35,7: 21,4: 42,9) 27, 28. Como vehículos, las formulaciones fueron preparadas sin PcAlCl. La concentración de PcAlCl se determinó por espectrofluorometría utilizando el fluorómetro LS 55 Perkin Elmer, UK; el espectro de excitación fue 670 nm y el de emisión 682 nm los resultados de concentración de PcAlCl fueron expresados en µM. El estado de agregación de PcAlCl en las formulaciones se determinó por fluorometría y por espectroscopía utilizando UV-Visible (UV-2401 PC Shimadzu, software UV Probe Vis). Los espectros de emisión y absorción de PcAlCl fueron graficados entre 250 y 800 nm.
Animales de Experimentación:
Se utilizaron ratas Wistar hembras de aproximadamente 2 meses de edad y 220 a 240 g de peso, obtenidas y mantenidas en el Bioterio Central del Departamento de Ciencias Básicas de la Universidad Industrial de Santander, según normativa establecida en la Ley 84, Capítulo 6 del 27 de Diciembre de 1989, emitida por el Congreso de Colombia 35 y en la Resolución 008430 de 1993, emitida por el Ministerio de Salud de la República de Colombia 36. La presente investigación contó con la aprobación del Comité de Ética de la Universidad Industrial de Santander, con código CB12006 en cuanto a la utilización de modelos animales para su desarrollo.
Ensayos de Difusión en Celdas de Franz:
Se utilizó piel dorsal de ratas Wistar como membrana. La piel fue extraída en un área entre 10 y 12 cm, se eliminó el tejido graso y la piel se cubrió con una película autosellante de Parafilm® M y papel aluminio. Los ensayos de difusión se llevaron a cabo utilizando celdas de Franz (PermeGear, Hellertown, PA, USA), siguiendo el protocolo descrito por Primo y col 31. En el compartimento receptor se colocaron 3 mL de búfer fosfato salino pH 7,2-SDS al 2% (PBS-SDS). Sobre el compartimento receptor se colocó la piel con el EC hacia el compartimento donador. Las celdas se colocaron en un agitador (Stirrer-PermeGear V6B, Hellertown, PA, USA) conectado a un baño recirculante (Lauda Brinkmann) a una temperatura de 32°C. Posteriormente, se colocó la cámara donadora y se colocaron 0,3 mL de las formulaciones (nano-PcAlCl: 200,13 µM y solución-PcAlCl: 100 µM). Se utilizaron seis celdas en cada ensayo. Los ensayos se llevaron a cabo por períodos de 12 y 24 horas. Se realizaron cuatro ensayos por cada formulación y en cada período. Los muestreos se realizaron en las horas 0, 2, 4, 8, 10 y 12, para ensayos a 12 horas y en las horas 0, 12, 14, 18, 22 y 24 para ensayos a 24 horas. Este muestreo se realizó extrayendo 0.3 mL del medio receptor; inmediatamente se repuso el mismo volumen de PBS-SDS. El volumen extraído se almacenó en tubos ámbar y posteriormente se realizó lectura de concentración de PcAlCl por fluorometría.
Cuantificación de PcAlCl en los Estratos de Piel:
Después de los ensayos de difusión, las membranas fueron retiradas y la retención en EC se determinó por el método de tape stripping, utilizando cinta Scotch Magic 3M (USA) según el protocolo descrito por Primo y col 31. Un trozo de cinta se pegó en la región central de cada piel, se ejerció presión por 30 segundos y se colocó en un tubo ámbar que contenía etanol al 70%. Este procedimiento se repitió con 15 cintas. La retención en epidermis más dermis (E+D), se determinó cortando la parte central de cada disco de piel en pequeños trozos con posterior macerado. Las muestras se colocaron en etanol al 70% por 12 horas. Se cuantificó la PcAlCl retenida por fluorometría.
DISTRIBUCIÓN DE PcAlCl EN PIEL Y ÓRGANOS DE RATAS WISTAR
Inducción de Lesiones Quirúrgicas y Aplicación del Tratamiento:
Después de la tricotomía los animales fueron anestesiados con xilacina y ketamina. Se hicieron dos cortes con tijeras y pinzas con el fin de romper las capas de la piel. Las lesiones midieron aproximadamente 5 mm de diámetro. Después de 30 minutos se aplicó Vetalgina como analgésico. Los animales con piel sana y con lesiones quirúrgicas inducidas, fueron divididos en grupos experimentales según lo descrito en la Tabla I. Las formulaciones fueron aplicadas en la piel de la región dorsal (área de 3 cm2) cada 24 horas durante ocho días.
TABLA I. Grupos experimentales en el ensayo de distribución de PcAlCl. Se muestran los grupos experimentales de animales con piel sana y animales con lesiones quirúrgicas inducidas, el tratamiento aplicado y la cantidad de animales utilizados en cada grupo experimental.
|
ANIMALES CON PIEL SANA |
||
|
Grupo |
Tratamiento |
Número de |
|
A |
Solución-PcAlCl |
5 |
|
B |
Vehículo-Solución |
2 |
|
C |
Nanoemulsión-PcAlCl |
5 |
|
D |
Vehículo-Nanoemulsión |
2 |
|
E |
Sin tratamiento |
2 |
|
ANIMALES CON LESIONES QUIRÚRGICAS INDUCIDAS |
||
|
Grupo |
Tratamiento |
Número de |
|
A |
Solución-PcAlCl |
4 |
|
B |
Vehículo-Solución |
4 |
|
C |
Nanoemulsión-PcAlCl |
4 |
|
D |
Vehículo-Nanoemulsión |
4 |
|
E |
Sin tratamiento |
4 |
Cuantificación de PcAlCl en Piel y Órganos:
Veinticuatro horas después de la última aplicación del tratamiento, los animales fueron anestesiados y luego de 10 minutos prefundidos, con solución salina a través del ventrículo cardíaco izquierdo. Se extrajo la piel (en el sitio de aplicación de las formulaciones y en un sitio distante de éste) y posteriormente el corazón, pulmón, hígado, bazo, riñón y cerebro. Se pesaron 300 mg de cada órgano y se maceraron con mortero y pistilo. Las muestras se trasladaron a tubos ámbar que contenían etanol al 70% y se mantuvieron en agitación constante durante 12 horas. Posteriormente, se realizó centrifugado a 3000 rpm durante 20 minutos, se colectó el sobrenadante y se realizó cuantificación del compuesto por fluorometría.
HISTOPATOLOGÍA DE LA PIEL
Se recolectaron biopsias de piel de las membranas utilizadas en las celdas de Franz y de la piel, en el sitio de aplicación de las formulaciones. Ellas fueron colocadas en formol tamponado al 10%. Posteriormente, fueron embebidas en bloques de parafina, se realizaron cortes histológicos con micrótomo RM2135 (Leica Microsystems®) y se ubicaron en láminas portaobjetos. Estas láminas pasaron por una serie de lavados con agua y alcoholes. Finalmente, fueron coloreadas con hematoxilina y eosina. Los resultados se registraron fotográficamente.
ANÁLISIS ESTADÍSTICO
Se realizó análisis de varianza (ANOVA) para el análisis de los ensayos ex vivo y la prueba de Kruskal-Wallis, seguida por la prueba de Mann-Whitney para los ensayos in vivo. El valor de significación estadística fue p<0,05. Los análisis se llevaron a cabo mediante el software SPSS versión 19.0.
RESULTADOS
Formulaciones de PcAlCl:
No hubo separación de fases ni agregados hasta dos meses después de la preparación de las formulaciones (nano-PcAlCl y solución-PcAlCl). Las dos formulaciones disueltas en DMSO y etanol presentaron un pico de emisión de fluorescencia a 680 nm y disueltas, en PBS-SDS presentaron dos picos de emisión uno a 670 nm y otro a 730 nm (Fig 1 A y B). En los espectros de absorción mostraron bandas Q con picos máximos entre 670 y 678 nm y bandas Soret entre 300 y 400 nm. Los espectros UV-VIS de la PcAlCl en DMSO y etanol fueron similares en cuanto a su comportamiento. En PBS-SDS las dos formulaciones presentaron muy baja absorción, sin embargo, el comportamiento del espectro se conservó, bandas Q más elevadas y bandas Soret más reducidas (Fig 1 C y D).
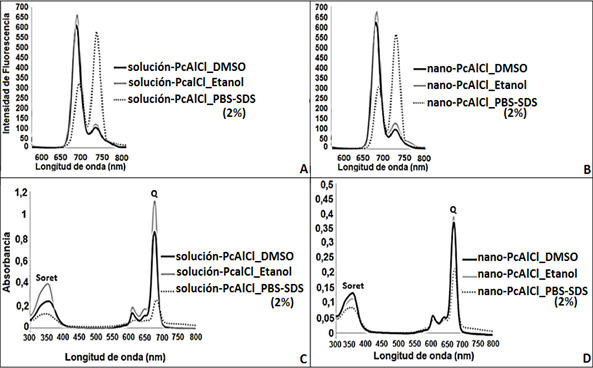
Fig 1. Espectros de emisión y absorción de PcAlCl. A) Espectro de emisión de PcAlCl en solución diluida en DMSO, etanol y PBS.SDS (2%). B) Espectro de emisión de PcAlCl en nanoemulsión diluida en DMSO, etanol y PBS.SDS (2%). C) Espectro de absorción de PcAlCl en solución diluida en DMSO, etanol y PBS.SDS (2%). D) Espectro de absorción de PcAlCl en nanoemulsión diluida en DMSO, etanol y PBS.SDS (2%). En C y D se observan las bandas Q y Soret de los espectros de absorción.
Difusión de PcAlCl en Piel de Ratas Wistar:
El tratamiento de las membranas con nano-PcAlCl y solución-PcAlCl, no presentó concentraciones detectables de PcAlCl en el medio receptor 12 y 24 horas post-tratamiento. La PcAlCl presente en las dos formulaciones no difundió a través de las capas de la piel hacia la cámara receptora del sistema utilizado. Este resultado se registró en los cuatro ensayos realizados, en cada tiempo y con cada formulación.
Cuantificación de PcAlCl en los Estratos de la Piel:
Los tratamientos con nano-PcAlCl y solución-PcAlCl indujeron la retención del compuesto en EC y en E+D de piel de ratas Wistar; esta retención fue dependiente del tiempo y de la formulación utilizada (Fig 2). En EC después de 12 horas de tratamiento las formulaciones NE y solución retuvieron 99,73 ± 2,41 y 66,73 ± 9,87 nM/cm2 de PcAlCl respectivamente. Después de 24 horas de tratamiento los valores de retención fueron menores, la NE retuvo 79,40 ± 3,42 nM/cm2 y la solución 57,01 ± 8,94 nM/cm2 de PcAlCl. En E+D post tratamiento con solución-PcAlCl se dio una retención de 81,92 ± 6,59 nM/cm2 a las 12 horas y 50,28 ± 5,00 nM/cm2 de PcAlCl a las 24 horas. Post tratamiento con nano-PcAlCl se obtuvo una retención de 40,94 ± 1,30 nM/cm2 después de 12 horas y 62,49 ± 2,39 nM/cm2 de PcAlCl después de 24 horas.
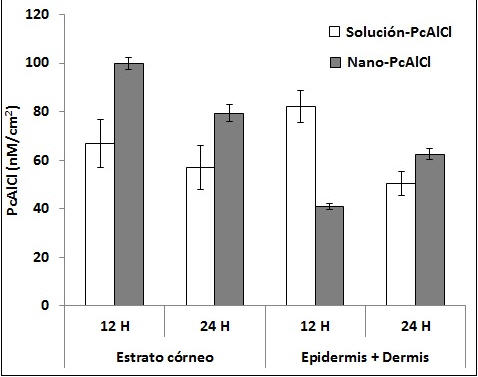
Fig 2. Retención de PcAlCl en piel de ratas Wistar. Retención en estrato córneo y epidermis más dermis después de 12 y 24 horas del inicio de los ensayos y de la aplicación de las formulaciones en las celdas de Franz.
Distribución de PcAlCl en Órganos de Ratas Wistar:
La PcAlCl se retuvo en el sitio de aplicación del tratamiento y en órganos, dependiendo de la integridad de la piel (piel sana o piel con lesión inducida) y de la formulación. En animales con piel sana (Fig 3 A) el tratamiento con nano-PcAlCl indujo mayor retención del compuesto en E+D, que en EC con valores de 33,18 ± 2,47 nM por mg de tejido y 6,43 ± 0,60 nM por mg de tejido respectivamente; no se encontraron concentraciones del compuesto en los órganos exceptuando el pulmón donde se registraron bajas concentraciones (0,82 ± 0,11 nM de PcAlCl por mg de tejido). El tratamiento con solución-PcAlCl presentó retención más elevada en E+D que en EC con valores de 202,40 ± 2,91 nM por mg de tejido y 31,86 ± 2,86 nM por mg de tejido, respectivamente. De igual forma los valores de concentración de PcAlCl registrados en pulmón fueron muy bajos (2,36 ± 0,45 nM de PcAlCl por mg de tejido). En animales con piel lesionada (Fig 3 B), el tratamiento con nano-PcAlCl indujo mayor retención en E+D (17,08 ± 1,47 nM por mg de tejido) que en EC (0,99 ± 0,13). En pulmón se registraron valores de concentración de 1,92 ± 0,12 nM por mg de tejido. El tratamiento con solución-PcAlCl también indujo una mayor retención en E+D (63,83 ± 2,07 nM por mg de tejido) que en EC (5,93 ± 0,25 nM por mg de tejido); en pulmón se registraron concentraciones de 20,33 ± 0,92 nM del compuesto por mg de tejido. La PcAlCl también se encontró en los demás órganos en orden descendente: hígado: 5,80 ± 1,20 nM por mg de tejido, bazo: 4,43 ± 0,29 nM por mg de tejido, corazón: 4,34 ± 0,32 nM por mg de tejido, cerebro: 1,98 ± 0,38 nM por mg de tejido y riñón: 1,57 ± 0,14 nM por mg de tejido. No se registró concentración de PcAlCl en ningún grupo experimental, después de la aplicación de los vehículos de las formulaciones ni en los animales que no recibieron tratamiento. En la piel distante del sitio de aplicación (piel no tratada) tampoco se presentó concentración del compuesto.
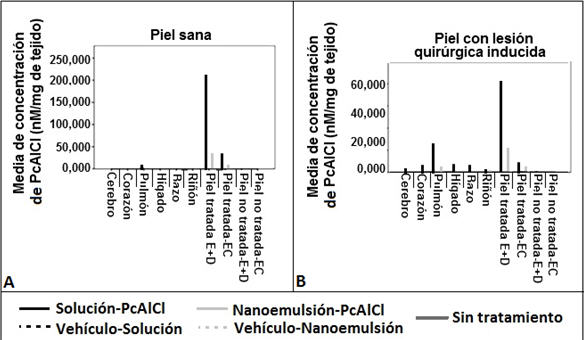
Fig 3. Distribución de PcAlCl en las capas de piel y en órganos de ratas Wistar con piel sana (A) y de piel con lesión quirúrgica inducida (B), después de la aplicación de las formulaciones y de los vehículos. Se registran los animales del grupo control que no recibieron tratamiento. En EC y E+D se realizaron lecturas de concentración tanto en piel del sitio de aplicación de los tratamientos (piel tratada) como en piel distante de este sitio (piel no tratada).
Características Histopatológicas de la Piel:
Las piel de ratas Wistar recién escindida (Fig 4 A y B) presentó una epidermis fina con epitelio plano estratificado queratinizado y una dermis formada por tejido conectivo laxo, fibroso, denso e irregular, con folículos pilosos, glándulas sebáceas y vasos sanguíneos. La epidermis y dermis se observaron estrechamente unidas. El colágeno presentó una morfología de fibras compactas formando una red. La piel analizada 12 horas después de los ensayos (Fig 4 C) mostró disminución en las capas del epitelio y disminución en número y en tamaño de las células de la epidermis. A las 24 horas presentó desprendimiento total del epitelio (Fig 4 D). En animales con piel sana la anatomía microscópica de este tejido fue normal (Fig 5 A). La piel de animales con lesiones inducidas quirúrgicamente (Fig 5 B, C y D), se caracterizó por presentar regeneración del epitelio. La epidermis presentó desprendimiento desorganizado de queratina, pérdida de diferenciación celular y en ocasiones, presencia de edema intercelular en las capas basal y granulosa. La dermis se caracterizó por presentar un infiltrado celular acompañado de neovascularización. La disposición de los vasos sanguíneos en formación de manera perpendicular a las fibras de colágeno, fue una de las principales características de la reparación y regeneración de este tejido.
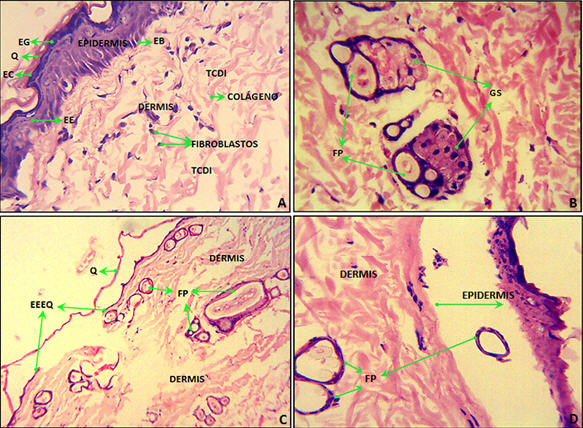
Fig 4. Anatomía microscópica de piel dorsal de ratas Wistar. A y B) Piel una vez escindida de los animales. Tinción hematoxilina-eosina (10X y 40X). C) Piel dorsal de ratas Wistar después de 12 horas de iniciados los ensayos de difusión y retención. Tinción hematoxilina-eosina (10X y 40X). D) Piel dorsal de ratas Wistar después de 24 horas de iniciados los ensayos de difusión y retención. Tinción hematoxilina-eosina (10X y 40X). (EC: Estrato córneo; EG: Estrato granuloso; EE: Estrato espinoso; EB: Estrato basal. Q: Queratina. TCDI: Tejido conectivo denso irregular. FP: Folículos pilosos. GS: Glándulas sebáceas. EEEQ: Epitelio estratificado escamoso queratinizado).
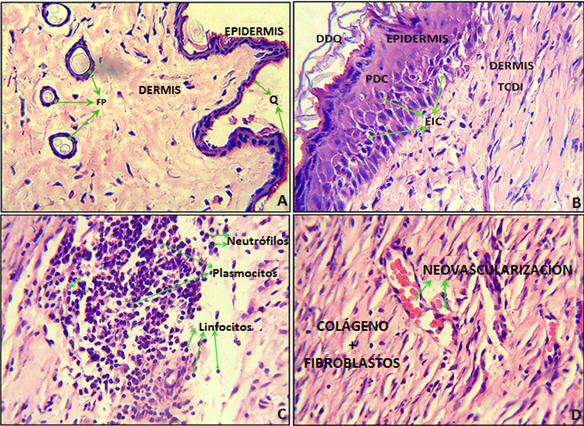
Fig 5. A) Anatomía microscópica de la piel extraída de animales sin lesión inducida (sitio de aplicación de las formulaciones). Tinción hematoxilina-eosina (10X y 40X). B, C y D) Caracterización microscópica de las lesiones inducidas quirúrgicamente en piel de ratas Wistar. Tinción hematoxilina-eosina (10X y 40X). Se muestran las capas de la piel: Epidermis y dermis y sus respectivas alteraciones debido a la lesión inducida. (Q: Queratina. TCDI: Tejido conectivo denso irregular. FP: Folículos pilosos. EIC: Edema intercelular. PDC: Pérdida de diferenciación celular. DDQ: Desprendimiento desorganizado de queratina.
DISCUSIÓN
Dado los inconvenientes de los tratamientos actuales en LC se requieren con urgencia nuevas terapias con bajos costos, menores efectos secundarios y mayor eficiencia 14, con el fin de optimizar una formulación de PcAlCl para ser utilizada en TFD como opción de tratamiento tópico en LC. En este trabajo se prepararon dos formulaciones conteniendo este compuesto, las que fueron retenidas en las capas de la piel y mostraron distribución in vivo, dependiendo de la formulación y la integridad de la piel en el sitio de aplicación. Los sistemas de liberación de fármacos (SLF) utilizados en TFD (en este caso para el tratamiento de LC) deben tener características como la entrega del compuesto en su forma activa a los sitios enfermos y también la penetración del EC hasta la dermis 37. De acuerdo con Peng y col 38, la agregación molecular acorta el tiempo de vida del estado triplete de las ftalocianinas y reduce el rendimiento de fluorescencia, lo que conduce a una disminución en la eficiencia de la TFD. Los espectros de absorción y emisión de un FS en diferentes solventes, proporcionan información sobre el estado agregado o monomérico de las moléculas del compuesto 37. En el presente estudio, los espectros de absorción y emisión de fluorescencia de la PcAlCl contenida en NE y en solución diluidas en solventes orgánicos, fueron característicos de ftalocianinas en estado no agregado. Sin embargo, cuando las formulaciones fueron diluidas en PBS-SDS la PcAlCl presentó una banda adicional de menor intensidad, que podría representar las moléculas en forma agregada. El cambio en la posición de las bandas, indicaría posiblemente que la longitud de onda de emisión es sensible a factores ambientales de los solventes. Ha sido reportado que al utilizar solventes con mayor polaridad, las bandas de emisión se desplazan en el espectro aumentando el valor de longitud de onda 39. Igual a lo hallado en este estudio, Rossetti y col 37 demostraron la formación de dímeros y agregados moleculares en medio acuoso con bandas Q y Soret amplias y una débil emisión de fluorescencia, en una microemulsión de ftalocianina de zinc diluida en agua; esta formulación diluida en DMSO no presentó estos agregados.
Encontramos que la PcAlCl no atravesó completamente las membranas sino que se retuvo en las diferentes capas de la piel, resultado considerado como positivo, ya que, el objetivo de esta formulación con PcAlCl es que el compuesto sea retenido en la dermis, sitio en el que se alojan los macrófagos parasitados por Leishmania 40. La permeación y difusión en sistemas ex vivo además de las propiedades fisicoquímicas del compuesto y del SLF utilizado, es afectada por factores como el tipo de animal y piel utilizada, las celdas de difusión utilizadas, el pre-tratamiento de la piel, factores ambientales 41 y la relación membrana/medio receptor utilizado 42. La PcAlCl es una molécula macrocíclica, hidrófoba, con peso molecular (574,96 g/mol) y coeficiente de partición octanol agua (7,3) elevados 43, que generalmente no penetra o es retenida sobre el EC. Por otra parte, es conocido que los surfactantes con mayor concentración como monoglicéridos, diglicéridos y polisorbato 80 (Tween 80) mejoran la penetración de compuestos hidrófilos pero no de compuestos lipófilos 44. El contenido de la fase acuosa también puede influenciar en la permeación; según Osborne y col 45, una microemulsión con bajo contenido de la fase acuosa, presentó baja capacidad para el transporte de glucosa a través de piel humana. Respecto del tipo de piel y el sistema ex vivo es posible, que la falta de microcirculación dérmica haya afectado la difusión del compuesto hacia las capas más profundas de la piel 41. Al utilizar una piel con EC, epidermis y dermisa polaridad de cada capa influye en el flujo de un compuesto dependiendo a su vez, de la polaridad de éste y de su SLF 46. Los cambios histológicos observados en las membranas después de los ensayos, muestran variaciones en este tejido causadas por la presión que ejerció la pinza de unión de las dos cámaras y por sobre-hidratación de la piel por el medio receptor. La entrada de agua en la membrana desde el medio receptor hacia las capas más profundas de la piel, se presentó en dirección opuesta a la entrada del compuesto desde las cámaras donadoras hacia este mismo sitio. Tanto la solución acuosa como las formulaciones se obstaculizan mutuamente y actúan como una barrera 46. Existen estudios de evaluación de permeación de NE utilizando diferentes tipos de piel. Primo y col 31, utilizando piel de oreja de cerdo y una NE magnética de Foscan, encontraron un perfil de liberación del compuesto luego de 4 horas del inicio del ensayo. Kong y col 47, utilizando piel de ratas Wistar y una NE conteniendo ácido hialurónico, encontraron liberación del compuesto hacia el medio receptor una hora después del inicio del ensayo. Por otra parte, Abu-Elyazid y col 3 utilizando piel abdominal de rata y una NE de Tenoxicam, encontraron liberación del compuesto después de dos horas de iniciado el ensayo.
La NE utilizada permitió la penetración de PcAlCl a través del EC y presentó liberación y retención del compuesto hacia las capas más profundas de la piel. Las nanoemulsiones poseen mejores propiedades para la permeación de compuestos, por las vías intercelulares y transcelulares del EC 48. Según Sanjula y col 48, un compuesto disuelto en el dominio lipídico de una NE, puede penetrar los lípidos del EC desestabilizando su estructura de bicapa. El dominio hidrófilo de la NE hidrata el EC e incrementa el volumen interlaminar de la bicapa lipídica. En la NE utilizada en este estudio el ácido oleico incrementó posiblemente la permeación, a través de vías no polares tal como fue demostrado por Larrucea y col 49, donde el ácido oleico incrementó la permeación y retención de Tenoxicam en las capas de la piel. Otros componentes de la NE como la fase acuosa, participan en la permeación y retención de compuestos a través de la hidratación del EC, el glicerol altera la estructura de la piel y difunde a través de ella, llevando también moléculas del compuesto hacia las capas viables 3; el DMSO facilita la difusión a través del EC y favorece la acumulación del compuesto en las capas más profundas de la piel 28 y el Tween 80 como agente tensoactivo no iónico y solvente de compuestos lipofílicos, mejora el flujo de fármacos a través de membranas biológicas 28,50.
La eficacia de la TFD en enfermedades cutáneas depende de la concentración del FS en el sitio terapéutico; al mismo tiempo, la seguridad del procedimiento se determina por los niveles del FS en los tejidos circundantes 51. Por lo tanto, la evaluación de la selectividad y acumulación del FS en el tejido blanco, así como su biodistribución en tejidos normales, es de gran importancia durante el desarrollo de nuevos FS y optimización de formulaciones con aplicación en TFD 52. La aplicación tópica de las formulaciones de PcAlCl en animales con piel normal limitó el compuesto al sitio de administración. La penetración del EC y la retención de la PcAlCl en E+D mostradas por las dos formulaciones ofrecen la probabilidad de ser utilizadas en TFD para LC. Una solución de PcAlCl mostró similares resultados en el modelo de cáncer 28. En los animales con piel lesionada la PcAlCl aplicada en NE también se retuvo en las capas viables. Los valores de retención más elevados fueron obtenidos post tratamiento con la solución de PcAlCl, debido probablemente a diferencias en las concentraciones del compuesto en las formulaciones utilizadas. Como lo indica Niazy y col 53, la concentración de un fármaco está directamente relacionada con su liberación transdérmica, a mayor concentración del compuesto mayor cantidad de este penetrado y liberado a través de la piel. En cuanto a la distribución de PcAlCl hacia el pulmón, se plantea la hipótesis que el compuesto haya sido inhalado por los animales y fue considerado en el estudio, como una variable no controlada que requiere ser analizada en estudios posteriores. Al respecto Young y col 54 considera que tras la inhalación, las partículas de un compuesto son liberadas desde los potenciadores de la permeación, contenidos en la formulación y directamente penetran el pulmón.
La PcAlCl no fue detectada en piel ni órganos de animales control. Como lo manifiestan Kyriazi y col 28 en su estudio farmacocinético de PcAlCl, este resultado confirma que no hubo moléculas biológicas en piel y órganos de ratas Wistar, ni en los solventes utilizados que afectaran la medida de fluorescencia de PcAlCl. La no presencia de PcAlCl en las muestras de piel, tomadas en un lugar distante del sitio de aplicación de los tratamientos, indica que la PcAlCl en NE y solución no presenta riesgo de fotosensibilidad generalizada. Contrario a las características de la piel de animales sanos, la piel de los animales con lesiones inducidas presentaron características similares a las observadas en lesiones por LC, donde se observa un infiltrado celular de macrófagos vacuolados en la dermis infectados con amastigotes, histiocitos, linfocitos y células plasmáticas y neutrófilos y eosinófilos en menor cantidad 8, 11, pérdida de estructuras anexiales 40 y daño en los estratos de la epidermis, originando la formación de una úlcera desprovista de EC10. Es importante, que la formulación de PcAlCl garantice la retención en piel y la no distribución del compuesto hacia órganos, evitando así fotosensibilidad generalizada. Con el desarrollo de este estudio se determinó que la NE utilizada es un SLF eficaz, para ser aplicada tópicamente debido a su capacidad para retener el compuesto en las capas viables de la piel, aún cuando estas capas presenten un daño y exhiban reparación y regeneración del tejido y por la ausencia de biodistribución. Se sugiere realizar ensayos en membranas de piel con remoción del EC, con el fin de simular el comportamiento de una piel con LC. También es recomendable realizar estudios de farmacocinética de PcAlCl, en modelos animales infectados con parásitos Leishmania, para tener conocimiento base sobre la seguridad de la PcAlCl, al ser aplicada en un organismo vivo con estas condiciones.
AGRADECIMIENTOS
El presente trabajo fue financiado por el Instituto Colombiano para el Desarrollo de la Ciencia y la Tecnología Francisco José de Caldas COLCIENCIAS, con código 110251929044 y la Universidad Industrial de Santander. Los autores agradecen al personal del Bioterio Central y del Laboratorio de Patología de la Universidad Industrial de Santander, a la Dra. Sandra Milena Leal por el apoyo en la preparación de las formulaciones y al Dr. Luis Carlos Orozco por el apoyo en el análisis estadístico.
1. Boada JN. Farmacología dermatológica. En: Flórez J, Armijo JA y Mediavilla A. Farmacología humana. Quinta Edición. Editorial Elsevier Masson. España. 2004; 1403-1422.
2. West DP y Micali G. Principles of Paediatric Dermatological Therapy. En: West DP y Micali G. Textbook of Pediatric Dermatology. Primera Edición. Blackwell Science Ltd. Oxford. 2000; 1731-1749.
3. Abu-Elyazid SK, Kassem AA, Samy AM, Gomaa ME. Evaluation of skin permeation and pharmacological effects of Tenoxicam nanoemulsion in topical formulations. Asian J Pharm Hea Sci 2011; 1: 99-105.
4. Primo FL, Rodrigues M, Simioni AR, Bentley MVLB, Morais PC, Tedesco AC. In vitro studies of cutaneous retention of magnetic nanoemulsion loaded with zinc phthalocyanine for synergic use in skin cancer treatment. J Magn Magn Mater 2008; 320: 211-214.
5. Steluti R, De Rosa FS, Collett J, Tedesco AC, Bentley MVLB. Topical glycerol monooleate/propylene glycol formulations enhance 5-aminolevulinic acid in vitro skin delivery and in vivo protophorphyrin IX accumulation in hairless mouse skin. Eur J Pharm Biopharm 2005; 60: 439-444.
6. Hadgraft J. Skin, the final frontier. Int J Pharm 2001; 224: 1-18.
7. El Maghraby GM, Barry BW, Williams AC. Liposomes and skin: From drug delivery to model membranes. Eur J Pharm Sci 2008; 34.
8. Silveira FT, Lainson R, Corbett CEP. Clinical and Immunopathological Spectrum of American Cutaneous Leishmaniasis with Special Reference to the Disease in Amazonian Brazil – A Review. Mem Inst Oswaldo Cruz 2004; 99 (3): 239-251.
9. Organización Mundial de la Salud (OMS). Control de la leishmaniasis. Resolución No EB 118/4 del consejo ejecutivo de la OMS. 2006; 1-7.
10. Calvopina M, Gómez EA, Uezato H, Kato H, Nonaka S, Hashiguchi Y. Atypical clinical variants in New World cutaneous leishmaniasis: disseminated, erysipeloid, and recidiva cutis due to Leishmania (V) panamensis. Am J Trop Med Hyg 2005; 73: 281-284.
11. Oliveira-Cardoso F, da Silva C, Gonçalvez V, Abreu-Silva AL, Gonçalves da Costa SC, da Silva Calabrese K. Inmunopathological studies of Leishmania amazonensis infection in resistant and in susceptible mice. J Infect Dis 2010; 12: 1933-1940.
12. Croft SL, Seifert K, Yardley V. Current scenario of drug development for leishmaniasis. Indian J Med Res 2006; 123: 399-410.
13. Croft SL, Coombs GH. Leishmaniasis – current chemotherapy and recent advances in the search for novel drugs. Trends Parasitol 2003; 19: 502-508.
14. Peloi LS, Biondo CE, Kimura E, Politi MJ, Lonardoni MV, Aristides SM, Dorea RC, Hioka N, Silveira TG. Photodynamic therapy for American cutaneous leishmaniasis: The efficacy of methylene blue in hamsters experimentally infected with Leishmania (Leishmania) amazonensis. Exp Parasitol 2011; 128: 353-356.
15. El-On J, Jacobs GP, Witztum E, Greenblatt CL. Development of topical treatment for cutaneous leishmaniasis caused by Leishmania major in experimental animals. Antimicrob Agents Chemother 1984; 26: 745-751.
16. Garnier T, Croft SL. Topical treatment for cutaneous leishmaniasis. Curr Opin Investig Drugs 2002; 3: 538-544.
17. Minodier P, Parola P. Cutaneous leishmaniasis treatment. Travel Med Infect Dis 2006; 5: 150-158.
18. Palumbo E. Current Treatment for Cutaneous Leishmaniasis: A Review. Am J Ther 2009; 16: 178-182.
19. Dutta S, Ray D, Kolli BK, Chang KP. Photodynamic sensitization of Leishmania amazonensis in both extracellular and intracellular stages with aluminium phthalocyanine chloride for photolysis in vitro. Antimicrob Agents Chemother 2005; 49: 4474-4484.
20. Castano AP, Demidova TN, Hamblin MR. Mechanisms in photodynamic therapy: part one-photosensitizers, photochemistry and cellular localization. Photodiagnosis Photodyn Ther 2004; 1(4): 279-293.
21. Levy JG. Photodynamic therapy. Trends Biotechnol 1995; 13: 14-18.
22. Machado AEH. Photodynamic Therapy: principles, potential of application and perspectives. Quim Nova 2000; 23: 237-243.
23. Akilov OE, Kosaka S, O’Riordan K, Song X, Sherwood M, Flotte TJ, Foley JW, Hasan T. The role of photosensitizer molecular charge and structure on the efficacy of photodynamic therapy against leishmania parasites. Chem Biol 2006; 13(8): 839-847.
24. Allen CM, Sharman WM, Van Lier JE. Current status of phthalocyanines in the photodynamic therapy of cancer. J Porphyr Phthalocyanines 2001; 5 (2): 161-169.
25. Rosenthal I. Phthalocyanine as photodynamic sensitizers. J Photochem Photobiol B 1991; 53: 859-870.
26. Escobar P, Hernández IP, Rueda CM, Martínez F, Páez E. Photodynamic activity of aluminum (III) and zinc (II) phthalocyanines in Leishmania promastigotes. Biomedica 2006; 26: 49-56.
27. Hernández IP. Actividad fototóxica in vitro e in vivo de ftalocianina de aluminio clorada contra Leishmania amazonensis. Tesis de maestría no publicada. Universidad Industrial de Santander. Colombia. 2010; 110.
28. Kyriazi M, Alexandratou E, Yova D, Rallis M, Trebst T. Topical photodynamic therapy of murine non-melanoma skin carcinomas with aluminum phthalocyanine chloride and a diode laser: pharmacokinetics, tumor response and cosmetic outcomes. Photodermatol Photoimmunol Photomed 2008; 24: 87-94.
29. Montanari J, Maidana C, Esteva MI, Salomon C, Morilla MJ, Romero EL. Sunlight triggered photodynamic ultradeformable liposomes against Leishmania braziliensis are also leishmanicidal in the dark. J Control Release 2010; 3: 368-373.
30. Vargas A, Eid M, Fanchaouy M, Gurny R, Delie F. In vivo photodynamic activity of photosensitizer-loaded nanoparticles: Formulation properties, administration parameters and biological issues involved in PDT outcome. Eur J Pharm Biopharm 2008; 69: 43-53.
31. Primo FL, Michieleto L, Rodrigues M, Macaroff PP, Morais PC, Lacava Z, Bentley MV, Tedesco AC. Magnetic nanoemulsions as drug delivery system for Foscan®: Skin permeation and retention in vitro assays for topical application in photodynamic therapy (PDT) of skin cancer. J Magn Mater 2007; 311: 354-357.
32. Sosnik A, Carcaboso AM, Glisoni RJ, Moretton MA, Chiappetta DA. New old challenges in tuberculosis: Potentially effective nanotechnologies in drug delivery. Adv Drug Deliv Rev 2010; 62: 547-559.
33. Fasolo D, Schwingel L, Holzschuh M, Bassani V, Teixeira H. Validation of an isocratic LC method for determination of quercetin and methylquercetin in topical nanoemulsions. J Pharm Biomed Anal 2007; 44: 1174-1177.
34. Garnier T, Mäntylä A, Järvinen T, Lawrence MJ, Brown MB, Croft SL. Topical buparvaquone formulations for the treatment of cutaneous leishmaniasis. J Pharm Pharmacol 2007; 59 (1): 41-49.
35. Colombia. Congreso de la República. Ley 84: Por la cual se adopta el Estatuto Nacional de Protección de los Animales, se crean unas contravenciones y se regula lo referente a su procedimiento y competencia. Diario Oficial No. 39120: Bogotá, DE. Colombia. 1989; 1-15.
36. Colombia. Ministerio de Salud. Resolución 008430: Por la cual se establecen las normas científicas, técnicas y administrativas para la investigación en salud. El Ministerio: Santafé de Bogotá, DC. Colombia; 1993; 21.
37. Rossetti FC, Lopes LB, Carollo AR, Thomazini JA, Tedesco AC, Bentley MV. A delivery system to avoid self-aggregation and to improve in vitro and in vivo skin delivery of a phthalocyanine derivative used in the photodynamic therapy. J Control Release 2011; 155: 400-408.
38. Peng Y, Zhang H, Wu H, Huang B, Gan L, Chen Z. The synthesis and photophysical properties of zinc (II) phthalocyanine bearing poly (aryl benzyl ether) dendritic substituents. Dyes Pigm 2010; 87: 10-16.
39. Rauf MA, Hisaindee S, Graham JP, Nawaz M. Solvent effects on the absorption and fluorescence spectra of Cu (II) – phthalocyanine and DFT calculations. J Mol Liq 2012; 168: 102-109.
40. Moskowitz PF, Kurban AK. Treatment of cutaneous leishmaniasis: retrospectives and advances for the 21st century. Clin Dermatol 1999; 17: 305-315.
41. Godin B, Touitou E. Transdermal skin delivery: predictions for humans from in vivo, ex vivo and animal models. Adv Drug Deliv Rev 2007; 59: 1152-1161.
42. Wagner H, Kostka KH, Lehr CM, Schaefer UF. Drug distribution in human skin using two different in vitro test systems: comparison with in vivo data. Pharm Res 2000; 12: 1475-1481.
43. Valdivieso W. Marcadores de apoptosis en Leishmania panamensis inducidos por la terapia fotodinámica utilizando ftalocianina de aluminio clorada como fotosensibilizador. Tesis de Maestría no publicada. Universidad Industrial de Santander. Colombia. 2010; 110.
44. Hosmer J, Reed R, Bentley MVLB, Nornoo A, Lopes LB. Microemulsions containing small-chain glycerides as transdermal delivery systems for hydrophilic and hydrophobic drugs. AAPS PharmSci Tech 2009; 10: 589-596.
45. Osborne DW, Ward AJ, O’Neill KJ. Microemulsions topical drug delivery vehicles: in-vitro transdermal studies a model hydrophilic drug. J Pharm Pharmacol 1991; 43: 450-454.
46. Wagner H, Kostka KH, Lehr CM, Schaefer UF. Interrelation of permeation and penetration parameters obtained from in vitro experiments with human skin and skin equivalents. J Control Release 2001; 75: 283-295.
47. Kong M, Guang Chen X, Keon D, Jin Park H. Investigations on skin permeation of hyaluronic acid based nanoemulsion as transdermal carrier. Carbohydr Polym 2011; 86: 837-843.
48. Sanjula B, Shakeel F, Ahuja A, Ali J, Shafiq S. Design, development and evaluation of novel nanoemulsion formulations for transdermal potential of celecoxib. Acta Pharm 2007; 57: 315-332.
49. Larrucea E, Arellano A, Santoyo S, Ygartua P. Combined effect of oleic acid and propylene glycol on the percutaneous penetration of tenoxicam and its retention in the skin. Eur J Pharm Biopharm 2001; 52: 113-119.
50. Williams AC, Barry BW. Penetration enhancers. Adv Drug Deliv Rev 2004; 56: 603-618.
51. Cheung R, Solonenko M, Busch TM, Del Piero F, Putt ME, Hahn SM, Yodh AG. Correlation of in vivo photosensitizer fluorescence and photodynamic-therapy-induced depth of necrosis in a murine tumor model. J Biomed Opt 2003; 8 (2): 248-252.
52. Shliakhtsin SV, Trukhachova TV, Isakau HA, Istomin YP. Pharmacokinetics and biodistribution of Photolon (Fotolon) in intact and tumor-bearing rats. Photodiagnosis Photodyn Ther 2009; 6: 97-104.
53. Niazy EM, Molokhia AM, El-Gorashi AS. Effect of vehicle and drug concentration on transdermal delivery of dihydroergotamine using excised animal skin. Drug Dev Ind Pharm 1990; 16: 1697-1715.
54. Young PM, Cocconi D, Colombo P, Bettini R, Price R, Steele DF, Tobyn MJ. Characterization of a surface modified dry powder inhalation carrier prepared by «particle smoothing». J Pharm Pharmacol 2002; 54: 1339-1344.
Referencias
REFERENCIAS
1. Boada JN. Farmacología dermatológica. En: Flórez J, Armijo JA y Mediavilla A. Farmacología humana. Quinta Edición. Editorial Elsevier Masson. España. 2004; 1403-1422.
2. West DP y Micali G. Principles of Paediatric Dermatological Therapy. En: West DP y Micali G. Textbook of Pediatric Dermatology. Primera Edición. Blackwell Science Ltd. Oxford. 2000; 1731-1749.
3. Abu-Elyazid SK, Kassem AA, Samy AM, Gomaa ME. Evaluation of skin permeation and pharmacological effects of Tenoxicam nanoemulsion in topical formulations. Asian J Pharm Hea Sci 2011; 1: 99-105.
4. Primo FL, Rodrigues M, Simioni AR, Bentley MVLB, Morais PC, Tedesco AC. In vitro studies of cutaneous retention of magnetic nanoemulsion loaded with zinc phthalocyanine for synergic use in skin cancer treatment. J Magn Magn Mater 2008; 320: 211-214.
5. Steluti R, De Rosa FS, Collett J, Tedesco AC, Bentley MVLB. Topical glycerol monooleate/propylene glycol formulations enhance 5-aminolevulinic acid in vitro skin delivery and in vivo protophorphyrin IX accumulation in hairless mouse skin. Eur J Pharm Biopharm 2005; 60: 439-444.
6. Hadgraft J. Skin, the final frontier. Int J Pharm 2001; 224: 1-18.
7. El Maghraby GM, Barry BW, Williams AC. Liposomes and skin: From drug delivery to model membranes. Eur J Pharm Sci 2008; 34.
8. Silveira FT, Lainson R, Corbett CEP. Clinical and Immunopathological Spectrum of American Cutaneous Leishmaniasis with Special Reference to the Disease in Amazonian Brazil – A Review. Mem Inst Oswaldo Cruz 2004; 99 (3): 239-251.
9. Organización Mundial de la Salud (OMS). Control de la leishmaniasis. Resolución No EB 118/4 del consejo ejecutivo de la OMS. 2006; 1-7.
10. Calvopina M, Gómez EA, Uezato H, Kato H, Nonaka S, Hashiguchi Y. Atypical clinical variants in New World cutaneous leishmaniasis: disseminated, erysipeloid, and recidiva cutis due to Leishmania (V) panamensis. Am J Trop Med Hyg 2005; 73: 281-284.
11. Oliveira-Cardoso F, da Silva C, Gonçalvez V, Abreu-Silva AL, Gonçalves da Costa SC, da Silva Calabrese K. Inmunopathological studies of Leishmania amazonensis infection in resistant and in susceptible mice. J Infect Dis 2010; 12: 1933-1940.
12. Croft SL, Seifert K, Yardley V. Current scenario of drug development for leishmaniasis. Indian J Med Res 2006; 123: 399-410.
13. Croft SL, Coombs GH. Leishmaniasis – current chemotherapy and recent advances in the search for novel drugs. Trends Parasitol 2003; 19: 502-508.
14. Peloi LS, Biondo CE, Kimura E, Politi MJ, Lonardoni MV, Aristides SM, Dorea RC, Hioka N, Silveira TG. Photodynamic therapy for American cutaneous leishmaniasis: The efficacy of methylene blue in hamsters experimentally infected with Leishmania (Leishmania) amazonensis. Exp Parasitol 2011; 128: 353-356.
15. El-On J, Jacobs GP, Witztum E, Greenblatt CL. Development of topical treatment for cutaneous leishmaniasis caused by Leishmania major in experimental animals. Antimicrob Agents Chemother 1984; 26: 745-751.
16. Garnier T, Croft SL. Topical treatment for cutaneous leishmaniasis. Curr Opin Investig Drugs 2002; 3: 538-544.
17. Minodier P, Parola P. Cutaneous leishmaniasis treatment. Travel Med Infect Dis 2006; 5: 150-158.
18. Palumbo E. Current Treatment for Cutaneous Leishmaniasis: A Review. Am J Ther 2009; 16: 178-182.
19. Dutta S, Ray D, Kolli BK, Chang KP. Photodynamic sensitization of Leishmania amazonensis in both extracellular and intracellular stages with aluminium phthalocyanine chloride for photolysis in vitro. Antimicrob Agents Chemother 2005; 49: 4474-4484.
20. Castano AP, Demidova TN, Hamblin MR. Mechanisms in photodynamic therapy: part one-photosensitizers, photochemistry and cellular localization. Photodiagnosis Photodyn Ther 2004; 1(4): 279-293.
21. Levy JG. Photodynamic therapy. Trends Biotechnol 1995; 13: 14-18.
22. Machado AEH. Photodynamic Therapy: principles, potential of application and perspectives. Quim Nova 2000; 23: 237-243.
23. Akilov OE, Kosaka S, O’Riordan K, Song X, Sherwood M, Flotte TJ, Foley JW, Hasan T. The role of photosensitizer molecular charge and structure on the efficacy of photodynamic therapy against leishmania parasites. Chem Biol 2006; 13(8): 839-847.
24. Allen CM, Sharman WM, Van Lier JE. Current status of phthalocyanines in the photodynamic therapy of cancer. J Porphyr Phthalocyanines 2001; 5 (2): 161-169.
25. Rosenthal I. Phthalocyanine as photodynamic sensitizers. J Photochem Photobiol B 1991; 53: 859-870.
26. Escobar P, Hernández IP, Rueda CM, Martínez F, Páez E. Photodynamic activity of aluminum (III) and zinc (II) phthalocyanines in Leishmania promastigotes. Biomedica 2006; 26: 49-56.
27. Hernández IP. Actividad fototóxica in vitro e in vivo de ftalocianina de aluminio clorada contra Leishmania amazonensis. Tesis de maestría no publicada. Universidad Industrial de Santander. Colombia. 2010; 110.
28. Kyriazi M, Alexandratou E, Yova D, Rallis M, Trebst T. Topical photodynamic therapy of murine non-melanoma skin carcinomas with aluminum phthalocyanine chloride and a diode laser: pharmacokinetics, tumor response and cosmetic outcomes. Photodermatol Photoimmunol Photomed 2008; 24: 87-94.
29. Montanari J, Maidana C, Esteva MI, Salomon C, Morilla MJ, Romero EL. Sunlight triggered photodynamic ultradeformable liposomes against Leishmania braziliensis are also leishmanicidal in the dark. J Control Release 2010; 3: 368-373.
30. Vargas A, Eid M, Fanchaouy M, Gurny R, Delie F. In vivo photodynamic activity of photosensitizer-loaded nanoparticles: Formulation properties, administration parameters and biological issues involved in PDT outcome. Eur J Pharm Biopharm 2008; 69: 43-53.
31. Primo FL, Michieleto L, Rodrigues M, Macaroff PP, Morais PC, Lacava Z, Bentley MV, Tedesco AC. Magnetic nanoemulsions as drug delivery system for Foscan®: Skin permeation and retention in vitro assays for topical application in photodynamic therapy (PDT) of skin cancer. J Magn Mater 2007; 311: 354-357.
32. Sosnik A, Carcaboso AM, Glisoni RJ, Moretton MA, Chiappetta DA. New old challenges in tuberculosis: Potentially effective nanotechnologies in drug delivery. Adv Drug Deliv Rev 2010; 62: 547-559.
33. Fasolo D, Schwingel L, Holzschuh M, Bassani V, Teixeira H. Validation of an isocratic LC method for determination of quercetin and methylquercetin in topical nanoemulsions. J Pharm Biomed Anal 2007; 44: 1174-1177.
34. Garnier T, Mäntylä A, Järvinen T, Lawrence MJ, Brown MB, Croft SL. Topical buparvaquone formulations for the treatment of cutaneous leishmaniasis. J Pharm Pharmacol 2007; 59 (1): 41-49.
35. Colombia. Congreso de la República. Ley 84: Por la cual se adopta el Estatuto Nacional de Protección de los Animales, se crean unas contravenciones y se regula lo referente a su procedimiento y competencia. Diario Oficial No. 39120: Bogotá, DE. Colombia. 1989; 1-15.
36. Colombia. Ministerio de Salud. Resolución 008430: Por la cual se establecen las normas científicas, técnicas y administrativas para la investigación en salud. El Ministerio: Santafé de Bogotá, DC. Colombia; 1993; 21.
37. Rossetti FC, Lopes LB, Carollo AR, Thomazini JA, Tedesco AC, Bentley MV. A delivery system to avoid self-aggregation and to improve in vitro and in vivo skin delivery of a phthalocyanine derivative used in the photodynamic therapy. J Control Release 2011; 155: 400-408.
38. Peng Y, Zhang H, Wu H, Huang B, Gan L, Chen Z. The synthesis and photophysical properties of zinc (II) phthalocyanine bearing poly (aryl benzyl ether) dendritic substituents. Dyes Pigm 2010; 87: 10-16.
39. Rauf MA, Hisaindee S, Graham JP, Nawaz M. Solvent effects on the absorption and fluorescence spectra of Cu (II) – phthalocyanine and DFT calculations. J Mol Liq 2012; 168: 102-109.
40. Moskowitz PF, Kurban AK. Treatment of cutaneous leishmaniasis: retrospectives and advances for the 21st century. Clin Dermatol 1999; 17: 305-315.
41. Godin B, Touitou E. Transdermal skin delivery: predictions for humans from in vivo, ex vivo and animal models. Adv Drug Deliv Rev 2007; 59: 1152-1161.
42. Wagner H, Kostka KH, Lehr CM, Schaefer UF. Drug distribution in human skin using two different in vitro test systems: comparison with in vivo data. Pharm Res 2000; 12: 1475-1481.
43. Valdivieso W. Marcadores de apoptosis en Leishmania panamensis inducidos por la terapia fotodinámica utilizando ftalocianina de aluminio clorada como fotosensibilizador. Tesis de Maestría no publicada. Universidad Industrial de Santander. Colombia. 2010; 110.
44. Hosmer J, Reed R, Bentley MVLB, Nornoo A, Lopes LB. Microemulsions containing small-chain glycerides as transdermal delivery systems for hydrophilic and hydrophobic drugs. AAPS PharmSci Tech 2009; 10: 589-596.
45. Osborne DW, Ward AJ, O’Neill KJ. Microemulsions topical drug delivery vehicles: in-vitro transdermal studies a model hydrophilic drug. J Pharm Pharmacol 1991; 43: 450-454.
46. Wagner H, Kostka KH, Lehr CM, Schaefer UF. Interrelation of permeation and penetration parameters obtained from in vitro experiments with human skin and skin equivalents. J Control Release 2001; 75: 283-295.
47. Kong M, Guang Chen X, Keon D, Jin Park H. Investigations on skin permeation of hyaluronic acid based nanoemulsion as transdermal carrier. Carbohydr Polym 2011; 86: 837-843.
48. Sanjula B, Shakeel F, Ahuja A, Ali J, Shafiq S. Design, development and evaluation of novel nanoemulsion formulations for transdermal potential of celecoxib. Acta Pharm 2007; 57: 315-332.
49. Larrucea E, Arellano A, Santoyo S, Ygartua P. Combined effect of oleic acid and propylene glycol on the percutaneous penetration of tenoxicam and its retention in the skin. Eur J Pharm Biopharm 2001; 52: 113-119.
50. Williams AC, Barry BW. Penetration enhancers. Adv Drug Deliv Rev 2004; 56: 603-618.
51. Cheung R, Solonenko M, Busch TM, Del Piero F, Putt ME, Hahn SM, Yodh AG. Correlation of in vivo photosensitizer fluorescence and photodynamic-therapy-induced depth of necrosis in a murine tumor model. J Biomed Opt 2003; 8 (2): 248-252.
52. Shliakhtsin SV, Trukhachova TV, Isakau HA, Istomin YP. Pharmacokinetics and biodistribution of Photolon (Fotolon) in intact and tumor-bearing rats. Photodiagnosis Photodyn Ther 2009; 6: 97-104.
53. Niazy EM, Molokhia AM, El-Gorashi AS. Effect of vehicle and drug concentration on transdermal delivery of dihydroergotamine using excised animal skin. Drug Dev Ind Pharm 1990; 16: 1697-1715.
54. Young PM, Cocconi D, Colombo P, Bettini R, Price R, Steele DF, Tobyn MJ. Characterization of a surface modified dry powder inhalation carrier prepared by «particle smoothing». J Pharm Pharmacol 2002; 54: 1339-1344.



