Autores | Contacto
D González1, J López Carchi 2, M Rodríguez 3, A Colque 4, G Faira 5, S Molina 6, R Zambrano 7, MG Vallone 8, MC Latorre 9, R Manzano 10, G Bendjuia 11 y DG Feinsilber 12
1 Médica Residente 2º año. División Dermatología. Hospital General de Agudos José María Ramos Mejía. danigmed@gmail.com
2 Médica Curso Superior 2º año. División Dermatología. Hospital General de Agudos José María Ramos Mejía. drajessica_lopez@hotmail.com
3 Médica Curso Superior 3º año. División Dermatología. Hospital General de Agudos José María Ramos Mejía. marianrodriguez5@hotmail.com
4 Médica Dermatóloga. División Dermatología. Hospital General de Agudos José María Ramos Mejía. anjeth@hotmail.com
5 Médica Dermatóloga. División Dermatóloga. Hospital General de Agudos José María Ramos Mejía. g_faira@hotmail.com
6 Médica Dermatóloga. División Dermatóloga. Hospital General de Agudos José María Ramos Mejía. msilmolina@hotmail.com
7 Médica Dermatóloga. División Dermatología. Hospital General de Agudos José María Ramos Mejía. rosmeryz@hotmail.com.
8 Médica Dermatóloga. Jefe de Residentes División Dermatología. Hospital General de Agudos José María Ramos Mejía. gabyvallone@hotmail.com
9 Médica Dermatóloga. Dirección del Registro Argentino de Melanoma Cutáneo (RAMC). Psoriahue. claralato@gmail.com
10 Médica Dermatóloga. Sector Colagenopatías. División Dermatología. Hospital General de Agudos José María Ramos Mejía. manzanoroxana@yahoo.com.ar
11 Médica Dermatóloga. Médica de Planta a cargo del Sector Colagenopatías. División Dermatología. Hospital General de Agudos José María Ramos Mejía. gbendjuia@yahoo.com.ar
12 Médico Dermatólogo. Jefe División Dermatología. Hospital General de Agudos José María Ramos Mejía. dafeinsilber@hotmail.com
Hospital General de Agudos José María Ramos Mejía. División Dermatología. Gral. Urquiza 609. Ciudad Autónoma de Buenos Aires. Argentina.
E-mail: colagenopatias@gmail.com.
Recibido: 10-04-2015
Aceptado para su Publicación: 29-05-2015
Dirección
Prof. Dr. Ricardo E. Achenbach
Resumen | Palabras Claves
RESUMEN
Objetivos: evaluar la utilidad práctica en nuestro medio del índice revisado de área y severidad del lupus cutáneo (RCLASI). Correlacionar RCLASI con DLQI (índice de calidad de vida dermatológico).
Materiales y Métodos: estudio observacional, descriptivo y transversal realizado en el Hospital General de Agudos José María Ramos Mejía, Ciudad Autónoma de Buenos Aires – Argentina – por dos grupos de observadores divididos según nivel de experiencia en dermatología. Se realizó RCLASI Y DLQI en 12 pacientes con Lupus Eritematoso Cutáneo (LEC). Se evaluó en RCLASI el tiempo requerido, la variabilidad inter-observador y la dificultad del método.
Resultados: la media de actividad para el grupo de baja experiencia fue de 11,8 puntos (SD 8,1) y para el de moderada / alta experiencia 12,7 (SD 8). La media de daño para el primer grupo fue 4 (SD 4,7) y para el segundo 4,4 puntos (SD 5,4), respectivamente. El tiempo promedio para ambos grupos fue de 7,76 minutos, siendo para el grupo de baja experiencia 9,79 y para el de moderada / alta 5,73. El método resultó fácil en más del 50% de los casos, independientemente del nivel de experiencia. El 50% de los pacientes no mostró efecto sobre la calidad de vida, 16,5% pequeño efecto, 25% moderado efecto y 8,5% gran efecto.
Conclusión: el RCLASI es un método práctico y útil para evaluar todas las formas de LEC. Resulta fácil y expeditivo, pero carece de escala de severidad, lo que fue una limitante para compararlo con DLQI.
PALABRAS CLAVE: Lupus; RCLASI; DLQI.
SUMMARY
Objectives: to assess the practical utility of Revised Cutaneous Lupus Erythematosus Disease Area and Severity Index (RCLASI) in our population. To correlate: RCLASI with DLQI (Dermatology Life Quality Index).
Materials and Methods: observational, descriptive and transversal study that was performed in Hospital General de Agudos José María Ramos Mejía, Ciudad Autónoma de Buenos Aires – Argentina – by two groups of observers divided by their level of experience in dermatology. RCLASI and DLQI were assessed in 12 patients with Cutaneous Lupus Erythematosus (CLE). Time spent, inter observer variability and method´s levels of difficulty were evaluated.
Results: the mean activity score for the group of low experience was 11,8 (SD 8,1) and for the group of moderate / high experience 12,7 (SD 8). The mean damage score for the former was 4 (SD 4,79) and for the later 4,4 (SD 5,4). The mean time spent by both groups was 7,76 minutes (9,79 minutes mean by the group of low experience and 5,73 by the group of moderate / high experience). The method was considered easy in more than 50% of the cases, independently of the observers´s level of experience. 50% of the patients did not show effect in their quality of life whereas 16,5% showed little effect, 25% mild effect, and 8,5% big effect.
Conclusions: RCLASI is a useful and feasible method to evaluate all types of CLE. It’s easy and rapid, however it lacks a severity scale. This later limited its comparison with DLQI.
KEY WORDS: Lupus; RCLASI; DLQI.
Artículo | Referencias
Descargar archivo PDF aquí
INTRODUCCIÓN
El control de las afecciones dermatológicas requiere, regularmente, de la evaluación de la actividad de la enfermedad y de su gravedad, con el fin de dar lugar a estrategias terapéuticas apropiadas.
El lupus eritematoso cutáneo (LEC) comprende un espectro de trastornos autoinmunes, que puede presentarse con una gran variedad de manifestaciones clínicas. 1,2,3 Durante décadas, en LEC sólo se utilizaron sistemas de medición no validados para evaluar la eficacia de los fármacos, aplicados en ensayos clínicos y la mayoría de estos estudios fueron pequeños y no controlados. 4
Los sistemas de medición han permitido a los médicos, cuantificar una enfermedad de manera reproducible. Tales sistemas han encontrado aplicaciones en la investigación clínica y juegan un papel cada vez más importante en la práctica dermatológica, donde utilizados regularmente, pueden ser útiles en el monitoreo de la enfermedad y así facilitar las decisiones terapéuticas. En el LEC, estos sistemas de puntuación, deben idealmente, proporcionar una evaluación precisa de todo el espectro de entidades clínicas. 4, 5, 6,7
Existen sistemas de puntuación para la evaluación del lupus eritematoso sistémico, como British Isles Lupus Assessment Group Index (BILAG), Safety of Estrogens in Lupus Erythematosus National Assessment (SELENA), Systemic Lupus Erythematosus Disease Activity Index (SLEDAI), Systemic Lupus Activity Measure (SLAM) y Systemic Lupus International Collaborating Clinics / American College of Rheumatology (SLICC/ACR) damage index (SDI) 8,9,10, sin embargo, estos scores no discriminan el compromiso órgano específico.
En 2005, Albrecht y col publicaron el primer instrumento de medición, validado para evaluar actividad y daño en LEC: the Cutaneous Lupus Erythematosus Disease Area and Severity Index (CLASI). 9,11,12 En su publicación original, Albrecht y col 13 mencionan que el CLASI ha sido diseñado como instrumento, para valorar los siguientes subtipos de LEC: lupus eritematoso discoide crónico (LEDC), lupus eritematoso cutáneo subagudo (LECSA) y lupus eritematoso sistémico (LES). Sin embargo, esta última entidad, no constituye en sí un LEC y puede ser mal interpretada, lo que llevó a los autores en publicaciones posteriores a sustituir el término «LES» por “LECA” (Lupus Eritematoso Cutáneo Agudo). 4,14,15
Teniendo en cuenta que el CLASI incluía datos subjetivos, aportados por el paciente y no evaluaba la presencia de signos relevantes para el LEC, como: induración y edema 16, Kuhn y col introdujeron una versión revisada del CLASI, el RCLASI (The Revised Cutaneous Lupus Erythematosus Disease Area and Severity Index). 17 El fin de dicha revisión fue mejorar el instrumento, por medio de la modificación de parámetros existentes y el agregado de nuevos, para permitir una evaluación específica de la severidad de la enfermedad, en todos lo subtipos de LEC. 9,18
Para medir cómo una enfermedad afecta la calidad de vida del individuo, se crearon los instrumentos de Calidad de Vida Relacionada con la Salud (CVRS). Si bien en el LE existen varios instrumentos que proporcionan una idea global, estos no son específicos para la problemática cutánea. 19,20 En contraposición, el Dermatology Life Quality Index (DLQI) 21 es un cuestionario de diez preguntas validado, utilizado en 40 enfermedades diferentes de la piel, que incluyen al LEC, en 80 países y más de 90 idiomas, con buena reproducibilidad y sensibilidad transcultural. 22, 23, 24, 25
OBJETIVOS
1. Evaluar la utilidad práctica en nuestro medio del RCLASI, en relación a factores tales como: el tiempo medio de realización, la variabilidad ínter- observador y la opinión del evaluador, según la dificultad para la realización del mismo.
2. Conocer los resultados del DLQI y correlacionar con los de RCLASI.
MATERIALES Y MÉTODOS
Se diseñó un estudio observacional, descriptivo y transversal evaluando los parámetros de RCLASI y DLQI, en pacientes con Lupus Eritematoso Cutáneo.
Se incluyeron doce pacientes mayores de 18 años, con diagnóstico de LEC según los criterios de Gillian 26, confirmado por la histopatología, cuya enfermedad se encontraba en actividad al momento del examen. Dichos pacientes consultaron al sector “Colagenopatías”, del Servicio de Dermatología del Hospital General de Agudos José María Ramos Mejía de la Ciudad de Buenos Aires, en el período comprendido entre enero de 2011 y abril de 2013. Todos los pacientes firmaron el consentimiento informado correspondiente.
Para cada paciente se evaluaron variables clínicas como: edad, sexo, tipo de lupus cutáneo y diagnóstico de otra enfermedad cutánea. En el estudio participaron siete observadores divididos en dos grupos: tres médicos dermatólogos en formación, que fueron clasificados como de baja experiencia (primero, segundo y tercer año de residencia en dermatología) y cuatro especialistas en dermatología, clasificados como de moderada / alta experiencia.
Se evaluó el RCLASI en todos los pacientes (ver Anexo I). Cabe resaltar, que ninguno de los observadores había utilizado este método previamente. Se cuantificó la actividad midiendo eritema, escama / hiperqueratosis, edema / infiltración, nódulos subcutáneos / placa, lesiones en las membranas mucosas, alopecia no cicatrizal y pelo lúpico (con un rango de 0 a 144 puntos) y el daño de la enfermedad, basándose en la presencia de discromía y cicatrices / atrofia (rango de 0 a 62 puntos).
Cada evaluador calificó de manera subjetiva, la complejidad en la realización del método en: fácil, de dificultad intermedia y difícil. Se cronometró, en minutos, el tiempo que demandó la realización del RCLASI.
Para medir la CVRS, todos los pacientes completaron el cuestionario DLQI (ver Anexo II). Este cuestionario consta de diez preguntas referidas a los últimos siete días, cuya puntuación total permite identificar los siguientes grupos: DLQI: 0-1 = ningún efecto en absoluto sobre la vida del paciente; 2-5 = pequeño efecto en la vida del paciente; 6-10 = efecto moderado sobre la vida del paciente; 11-20 = gran efecto en la vida del paciente; 21 a 30 = muy grande efecto en la vida del paciente.
ANEXO I. RCLASI. 17

ANEXO II. Tabla DLQI.22

ANÁLISIS Y RESULTADOS
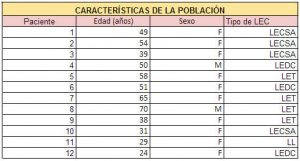
Para el presente trabajo se incluyeron doce pacientes (10 mujeres y 2 varones). La media de edad al momento del estudio fue 46,5 +/- 14,5 (rango 24-70). Cuatro pacientes correspondían a formas de Lupus Eritematoso Cutáneo Subagudo (LECSA), cuatro a lupus Eritematoso Tumidus (LET), tres a Lupus Eritematoso Discoide Crónico (LEDC) y sólo un paciente presentaba el subtipo Lupus Liquen (LL). El 25% (tres) había presentado otro tipo de Lupus Eritematoso Cutáneo (LEC), sin actividad al momento de la evaluación (paniculitis, lupus sabañón y LEDC). EL 50% de los pacientes (seis) presentaban además, diagnóstico de otra enfermedad cutánea diferente del LEC, al momento de la evaluación: livedo racemoso, acrocianosis, pigmentación postinflamatoria y rosácea (Tabla I).
TABLA I. Características de la población
Para el total de pacientes, la media de la actividad de la enfermedad según el RCLASI varió de 3,6 a 26,4 puntos, mientras que la media de daño varió de 0 a 16,4 puntos.
La media del total de actividad para el grupo de baja experiencia fue de 11,8 (DS 8,1), en comparación con el grupo de moderada / alta experiencia 12,7 (DS 8). En cuanto a la media del total de daño para el primer grupo fue 4 (DS 4,7) y el segundo 4,4 (DS 5,4) (Gráfico I).
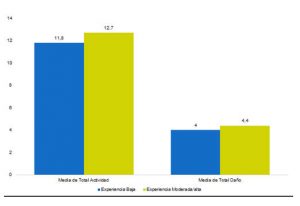
GRÁFICO I. Media de RCLASI según experiencia
El tiempo promedio en minutos, que demandó la realización del score para ambos grupos de evaluadores fue de 7,76, siendo para el grupo de baja experiencia 9,79 y para el de moderada / alta 5,73. El tiempo medio consumido por evaluador, varió significativamente con un rango de 3,6 a 14,7 min, con el mayor tiempo consumido por un evaluador con baja experiencia y el menor tiempo, por profesionales de mayor experiencia (Gráfico II).
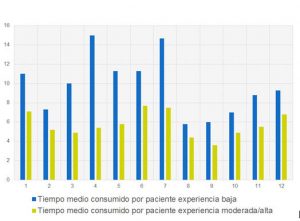
GRÁFICO II. Tiempo medio en minutos para RCLASI
La opinión del evaluador, sobre la complejidad del método en el grupo de baja experiencia, resultó fácil en el 52,7%, de dificultad intermedia en el 30,6%, difícil en el 16,7% y los de experiencia moderada / alta obtuvieron un 68,7 %, 25 % y 6,3 % respectivamente (Gráfico III).
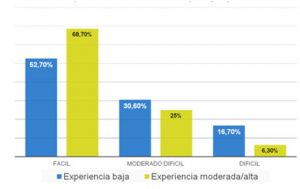
GRÁFICO III. Opinión del RCLASI por grupos de observadores
En relación al DLQI, la media para todos los pacientes fue de 3,83 puntos. Cuando se analizó el índice por grupos, el 50% (seis) de los pacientes no presentaron ningún efecto sobre la calidad de vida, 16,5% (dos) de los pacientes tuvieron pequeño efecto en la calidad de vida, 25% (tres) moderado efecto y 8,5% (uno) gran efecto (Gráfico IV).
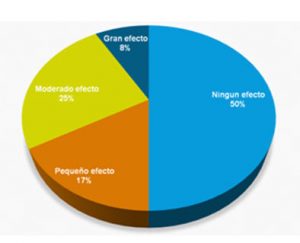
GRÁFICO IV. Efecto sobre la calidad de vida
DISCUSIÓN
En LEC es importante evaluar, tanto el grado de actividad como el de daño de manera apropiada; esto hace necesario la implementación de métodos confiables, rápidos y reproducibles en la práctica clínica.
El RCLASI, a diferencia de otros métodos 5,8,13,14, toma en cuenta la mayoría de las manifestaciones clínicas del espectro de esta enfermedad 15,17,18,27. Esta versión revisada y clínicamente validada, añade parámetros como: edema / infiltración, nódulos / placas subcutáneas, área de los labios, para evaluar lesiones específicas de LED y LECSA, “lipoatrofia” para daño en la sección cicatriz / atrofia y un nuevo párrafo llamado “pelo lúpico” o “lanugo” para evaluar actividad en alopecia. Asimismo, se aumentó la precisión de parámetros existentes, tales como: escama / hipertrofia, alteraciones de la pigmentación, cicatrices / atrofia / paniculitis y se modificó la puntuación de daño en alopecia cicatrizal, al estimar un porcentaje para cada área comprometida. Estas modificaciones sensibilizan la determinación de actividad. 17,27 Además, reduce la posibilidad de sesgo 8, ya que, no incluye en la puntuación total, la valoración subjetiva del paciente respecto de la existencia de lesiones mucosas, al tiempo de evolución de la discromía, así como, de la caída de cabello. 18,27,28 Esto nos permitió valorar diferentes tipos de LEC como: LECSA, LEDC, LL y especialmente al LT, cuyas características clínicas son subvaloradas en otros scores. 16
En nuestro estudio, el tiempo medio consumido por evaluador varió en un rango de 4 a 13,2 min, con una media de 7,76 min. Estas mediciones fueron mayores en comparación con la publicación de Kuhny col, 17 donde dicho rango varió entre 3,02 a 4,34 min con una media de 3,75 min. Podemos inferir que esta diferencia en el tiempo, se podría deber a que la proporción de evaluadores con alta experiencia, fue menor a la usada en dicho estudio. Por otro lado, en nuestro grupo de baja experiencia en el ejercicio de la dermatología, el tiempo requerido fue mayor respecto del de alta experiencia (9,79 vs 5,73 minutos). Es interesante que en una segunda evaluación, Kuhny col 17notaron una disminución significativa del tiempo requerido para la realización del score, por lo que podríamos suponer, que el uso cotidiano de este instrumento optimizaría esta variable. Si se toma como referencia el Score CLASI, aquí el tiempo medio fue de 5,7 min. 4,13
Tal como se observó en otros estudios 17, no encontramos variabilidad inter-observador al analizar actividad y daño. De hecho, para el grupo de baja experiencia, la media de actividad fue de 11,8 (DS 8,1) y de daño fue de 3,6 (DS 4,7) en comparación con el grupo de moderada / alta experiencia que fue de 14,7 (DS 8) y de 4,4 (DS 5,4) respectivamente.
Cuando analizamos la opinión del evaluador acerca de la complejidad del método, el 52,7% de las evaluaciones resultaron fáciles para el grupo de baja experiencia, y el 68,7 % para el grupo de moderada / alta. El interés de conocer la evaluación subjetiva del observador, es inferir la utilidad práctica del método en la consulta diaria y reconocer si esta varía, de acuerdo con la experiencia del observador. En cuanto a la bibliografía, la opinión del evaluador está referida al diseño estructural del score y no a su opinión global. 4,17
El DLQI es el cuestionario más utilizado en dermatología, ya que, es más específico para enfermedades cutáneas, fácil de realizar, reproducible y existe una versión validada en español. 22 Estas fueron las razones que nos llevaron a seleccionar el DLQI en este estudio.
En nuestro trabajo, el DLQI promedio para todos los pacientes fue de 3,83 puntos, que se corresponde con una afección leve en la calidad de vida. Ferraz y col, evaluaron la calidad de vida en 71 pacientes con lupus eritematoso y lesiones cutáneas, siendo la puntuación media del DLQI de 6,5. 29 En la población analizada, el 50% no presentaba ningún efecto en la calidad de vida, a diferencia de lo descrito en la bibliografía 19, 20, 30 y particularmente, por Batalla y col 31 donde el impacto fue moderado, grande o extremadamente grande en el 50% de los pacientes con LEC.
Por otro lado, no pudimos correlacionar el DLQI con RCLASI, ya que, para este último aún no se han definido grados de severidad. Otros autores, no encontraron asociaciones entre la puntuación del DLQI y la gravedad de la enfermedad, medida con CLASI o describen una correlación débil, entre los puntajes de actividad de la enfermedad con las puntuaciones de calidad de vida. 8,31 Sin embargo, en algunos pacientes con gran afección de la calidad de vida el DLQI, juega un papel importante en la toma de decisiones terapéuticas.
Encontramos como limitantes para nuestro estudio el tamaño de la muestra, lo que no nos permitió evaluar influencia en el tiempo consumido, en relación con el tipo de lupus cutáneo, la distribución topográfica y la experiencia. Por otro lado, al carecer de una escala apropiada para clasificar la severidad de RCLASI en leve, moderado y severo, no se pudo establecer una correlación entre la severidad de LEC y la repercusión de éste, en la calidad de vida de los pacientes.
CONCLUSIÓN
En nuestro estudio el RCLASI resultó un método práctico, útil y reproducible para evaluar todas las formas de LEC.
Queda pendiente desarrollar una escala de severidad para el RCLASI, tal como existe en el CLASI, para lo que sería necesario realizar un proyecto multicéntrico que permita diseñarla y validarla. Esto posibilitaría, entre otras cosas, correlacionar los resultados del RCLASI con CVRS.
Glosario
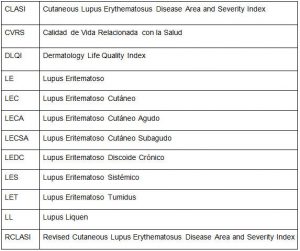
1. Obermoser G, Sontheimer RD, Zelger B. Overview of common, rare and atypical manifestations of cutaneous lupus erythematosus and histopathological correlates. Lupus 2010; 19: 1050-1070.
2. Kuhn A, Landmann A. The classification and diagnosis of cutaneous lupus erythematosus. J Autoimmun 2014; 48-49: 14-19.
3. Moura JP Filho, Peixoto RL, Martins LG, Melo SD, Carvalho LL, Pereira AK, Freire EA. Lupus erythematosus: considerations about clinical, cutaneous and therapeutic aspects. An Bras Dermatol 2014; 89 (1): 118-125.
4. Albrecht J, Werth VP. Development of the CLASI as an outcome instrument for cutaneous lupus erythematosus. Dermatol Ther 2007; 20: 93-101.
5. Abdel-Aziz K, Goodfield M. Evaluation of the Cutaneous Lupus Activity and Severity Score in the assessment of lupus erythematosus skin disease. Br J Dermatol 2008; 158: 181-182.
6. Klein R, Moghadam-kia SL, Monico J, Okawa J, Coley C, Taylor L, Troxel AB, Werth VP. Development of the CLASI as a tool to measure disease severity and responsiveness to therapy in cutaneous lupus erythematosus. Arch Dermatol 2011; 147 (2): 203-208.
7. Goodfield M. Measuring the activity of disease in cutaneous lupus erythematosus. Br J Dermatol 2000; 142: 399-400.
8. Wahie S, Mc Coll E, Reynolds NJ, Meggit SJ. Measuring disease activity and damage in discoid lupus erythematosus. Br J Dermatol 2010; 162: 1030-1037.
9. Jolly M, Kazmi N, Mikolaitis RA, Sequeira W, Block JA. Validation of the Cutaneous Lupus Disease Area and Severity Index (CLASI) using physician – and patient – assessed health outcome measures. J Am Acad Dermatol 2013; 68 (4): 618-623.
10. Parodi A, Massone C, Cacciapuoti M y col. Measuring the activity of the disease in patients with cutaneous lupus erythematosus. Br J Dermatol 2000; 142: 457-460.
11. Jolly M, Mikolaitis R, Cash T, Block J. Validation of CLASI scale with lupus disease activity, damage, body image and quality of life (abstract). Arthritis Rheum 2010; 62 (10s): 1880.
12. Krathen MS, Dunham J, Gaines E, Junkins-Hopkins J, Kim E, Kolasinski SL y col. The Cutaneous Lupus Erythematosus Disease Activity and Severity Index: expansion for rheumatology and dermatology. Arthritis Rheum 2008; 59: 338-344.
13. Albrecht J, Taylor L, Berlin JA y col. The CLASI (Cutaneous Lupus Disease Area and Severity Index): an outcome instrument for cutaneous lupus erythematosus. J Invest Dermatol 2005; 125: 889-894.
14. Albrecht J, Werth VP. Clinical outcome measures for cutaneous lupus erythematosus. Lupus 2010; 19: 1137-1143.
15. Bonilla-Martínez ZL, Albrecht J, Troxel AB y col. The cutaneous lupus erythematosus disease area and severity index: a responsive instrument to measure activity and damage in patients with cutaneous lupus erythematosus. Arch Dermatol 2008; 144 (2): 173-180.
16. Bein D, Kuehn E, Meuth AM, Amler S, Haust M y col. Evaluation of disease activity and damage in different subtypes of cutaneous lupus erythematosus using the CLASI. J Eur Acad Dermatol Venereol 2011; 25 (6): 652-659.
17. Kuhn A, Amler S, Beissert S, Bohm M, Brehler R, Ehrchen J y col. Revised Cutaneous Lupus Erythematosus Disease Area and Severity Index (RCLASI): a modified outcome instrument for cutaneous lupus erythematosus. Br J Dermatol 2010; 163: 83-92.
18. Kreuter A. A revised scoring system for cutaneous lupus erythematosus: the RCLASI. Br J Dermatol 2010; 163: 3.
19. Jones-Caballero M, Peñas PF, García-Diez A, Chren MM, Badía X. The Spanish version of Skindex-29. An instrument for measuring quality of life in patients with cutaneous diseases. Med Clin (Barc) 2002; 118 (1): 5-9.
20. Gaines E, Bonilla-Martínez Z, Albrecht J, Taylor L, Okawa J, Troxel AB y col. Quality of life and disease severity in a cutaneous lupus erythematosus pilot study. Arch Dermatol 2008; 144: 1061-1062.
21. Finlay AY, Khan GK. Dermatology Life Quality Index (DLQI) – a simple practical measure – for routine clinical use. Clin Exp Dermatol 1994; 19: 210-216.
22. Tiedra A, Mercadal J, Badía X, Mascaró JM, Herdman M, Lozano R. Adaptación transcultural al español del cuestionario Dermatology Life Quality Index (DLQI): el índice de calidad de vida en Dermatología. Actas Dermosifiliogr 1998; 89: 692-700.
23. Finlay AY, Khan GK. Dermatology Life Quality Index (DLQI): a simple practical measure for routine clinical use. Clin Exp Dermatol 1994; 19: 210-216.
24. Ludwig MWB, Oliveira MSO, Müller MC, Moraes JD. Qualidade de vida e localização da lesão em pacientes dermatológicos. An Bras Dermatol 2009; 84 (2): 143-150.
25. Ferraz LB, Almeida FA, Vasconcellos MR, Faccina AS, Ciconelli RM, Ferraz MB. The impact of lupus erythematosus cutaneous on the Quality of life: the Brazilian- Portuguese version of DLQI. Qual Life Res 2005; 15: 546-570.
26. Gilliam JN, Sontheimer RD. Skin manifestations of SLE. Clin Rheum Dis 1982; 8: 207-218.
27. Kuhn A, Ruland V, Bonsmann G. Measuring disease activity and damage in cutaneous lupus erythematosus: reply from authors. Br J Dermatol 2011; 164 (1): 222-224.
28. Charman C, Chambers C, Williams H. Measuring atopic dermatitis severity in randomized controlled clinical trials: what exactly are we measuring? J Invest Dermatol 2003; 120: 932-941.
29. Ferraz LB, de Almeida FA, Vasconcellos MR, Ferraz MB. Alopecia impairs the quality of life of patients with lupus erythematosus. Arch Dermatol 2006; 142: 110.
30. Vásquez R, Wang D, Tran QP, Adams-Huet B, Chren MM, Costner MI y col. A multi-center, cross-sectional study on quality of life in cutaneous lupus erythematosus patients. Br J Dermatol 2013; 168: 145-153.
31. Batalla A, García-Doval I, Peón G, de la Torre C. Estudio de la calidad de vida en pacientes con lupus eritematoso cutáneo. Actas Dermosifiliogr 2013; 104: 800-806.
Referencias
REFERENCIA
1. Obermoser G, Sontheimer RD, Zelger B. Overview of common, rare and atypical manifestations of cutaneous lupus erythematosus and histopathological correlates. Lupus 2010; 19: 1050-1070.
2. Kuhn A, Landmann A. The classification and diagnosis of cutaneous lupus erythematosus. J Autoimmun 2014; 48-49: 14-19.
3. Moura JP Filho, Peixoto RL, Martins LG, Melo SD, Carvalho LL, Pereira AK, Freire EA. Lupus erythematosus: considerations about clinical, cutaneous and therapeutic aspects. An Bras Dermatol 2014; 89 (1): 118-125.
4. Albrecht J, Werth VP. Development of the CLASI as an outcome instrument for cutaneous lupus erythematosus. Dermatol Ther 2007; 20: 93-101.
5. Abdel-Aziz K, Goodfield M. Evaluation of the Cutaneous Lupus Activity and Severity Score in the assessment of lupus erythematosus skin disease. Br J Dermatol 2008; 158: 181-182.
6. Klein R, Moghadam-kia SL, Monico J, Okawa J, Coley C, Taylor L, Troxel AB, Werth VP. Development of the CLASI as a tool to measure disease severity and responsiveness to therapy in cutaneous lupus erythematosus. Arch Dermatol 2011; 147 (2): 203-208.
7. Goodfield M. Measuring the activity of disease in cutaneous lupus erythematosus. Br J Dermatol 2000; 142: 399-400.
8. Wahie S, Mc Coll E, Reynolds NJ, Meggit SJ. Measuring disease activity and damage in discoid lupus erythematosus. Br J Dermatol 2010; 162: 1030-1037.
9. Jolly M, Kazmi N, Mikolaitis RA, Sequeira W, Block JA. Validation of the Cutaneous Lupus Disease Area and Severity Index (CLASI) using physician – and patient – assessed health outcome measures. J Am Acad Dermatol 2013; 68 (4): 618-623.
10. Parodi A, Massone C, Cacciapuoti M y col. Measuring the activity of the disease in patients with cutaneous lupus erythematosus. Br J Dermatol 2000; 142: 457-460.
11. Jolly M, Mikolaitis R, Cash T, Block J. Validation of CLASI scale with lupus disease activity, damage, body image and quality of life (abstract). Arthritis Rheum 2010; 62 (10s): 1880.
12. Krathen MS, Dunham J, Gaines E, Junkins-Hopkins J, Kim E, Kolasinski SL y col. The Cutaneous Lupus Erythematosus Disease Activity and Severity Index: expansion for rheumatology and dermatology. Arthritis Rheum 2008; 59: 338-344.
13. Albrecht J, Taylor L, Berlin JA y col. The CLASI (Cutaneous Lupus Disease Area and Severity Index): an outcome instrument for cutaneous lupus erythematosus. J Invest Dermatol 2005; 125: 889-894.
14. Albrecht J, Werth VP. Clinical outcome measures for cutaneous lupus erythematosus. Lupus 2010; 19: 1137-1143.
15. Bonilla-Martínez ZL, Albrecht J, Troxel AB y col. The cutaneous lupus erythematosus disease area and severity index: a responsive instrument to measure activity and damage in patients with cutaneous lupus erythematosus. Arch Dermatol 2008; 144 (2): 173-180.
16. Bein D, Kuehn E, Meuth AM, Amler S, Haust M y col. Evaluation of disease activity and damage in different subtypes of cutaneous lupus erythematosus using the CLASI. J Eur Acad Dermatol Venereol 2011; 25 (6): 652-659.
17. Kuhn A, Amler S, Beissert S, Bohm M, Brehler R, Ehrchen J y col. Revised Cutaneous Lupus Erythematosus Disease Area and Severity Index (RCLASI): a modified outcome instrument for cutaneous lupus erythematosus. Br J Dermatol 2010; 163: 83-92.
18. Kreuter A. A revised scoring system for cutaneous lupus erythematosus: the RCLASI. Br J Dermatol 2010; 163: 3.
19. Jones-Caballero M, Peñas PF, García-Diez A, Chren MM, Badía X. The Spanish version of Skindex-29. An instrument for measuring quality of life in patients with cutaneous diseases. Med Clin (Barc) 2002; 118 (1): 5-9.
20. Gaines E, Bonilla-Martínez Z, Albrecht J, Taylor L, Okawa J, Troxel AB y col. Quality of life and disease severity in a cutaneous lupus erythematosus pilot study. Arch Dermatol 2008; 144: 1061-1062.
21. Finlay AY, Khan GK. Dermatology Life Quality Index (DLQI) – a simple practical measure – for routine clinical use. Clin Exp Dermatol 1994; 19: 210-216.
22. Tiedra A, Mercadal J, Badía X, Mascaró JM, Herdman M, Lozano R. Adaptación transcultural al español del cuestionario Dermatology Life Quality Index (DLQI): el índice de calidad de vida en Dermatología. Actas Dermosifiliogr 1998; 89: 692-700.
23. Finlay AY, Khan GK. Dermatology Life Quality Index (DLQI): a simple practical measure for routine clinical use. Clin Exp Dermatol 1994; 19: 210-216.
24. Ludwig MWB, Oliveira MSO, Müller MC, Moraes JD. Qualidade de vida e localização da lesão em pacientes dermatológicos. An Bras Dermatol 2009; 84 (2): 143-150.
25. Ferraz LB, Almeida FA, Vasconcellos MR, Faccina AS, Ciconelli RM, Ferraz MB. The impact of lupus erythematosus cutaneous on the Quality of life: the Brazilian- Portuguese version of DLQI. Qual Life Res 2005; 15: 546-570.
26. Gilliam JN, Sontheimer RD. Skin manifestations of SLE. Clin Rheum Dis 1982; 8: 207-218.
27. Kuhn A, Ruland V, Bonsmann G. Measuring disease activity and damage in cutaneous lupus erythematosus: reply from authors. Br J Dermatol 2011; 164 (1): 222-224.
28. Charman C, Chambers C, Williams H. Measuring atopic dermatitis severity in randomized controlled clinical trials: what exactly are we measuring? J Invest Dermatol 2003; 120: 932-941.
29. Ferraz LB, de Almeida FA, Vasconcellos MR, Ferraz MB. Alopecia impairs the quality of life of patients with lupus erythematosus. Arch Dermatol 2006; 142: 110.
30. Vásquez R, Wang D, Tran QP, Adams-Huet B, Chren MM, Costner MI y col. A multi-center, cross-sectional study on quality of life in cutaneous lupus erythematosus patients. Br J Dermatol 2013; 168: 145-153.
31. Batalla A, García-Doval I, Peón G, de la Torre C. Estudio de la calidad de vida en pacientes con lupus eritematoso cutáneo. Actas Dermosifiliogr 2013; 104: 800-806.